
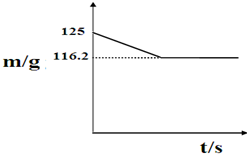
 兴趣小组的同学们从山上采集到一种石灰石(主要成分为碳酸钙),他们将25克该样品放入盛有100g稀盐酸的烧杯中,恰好完全反应(杂质不与稀盐酸反应,也不溶于水),测得反应后烧杯中剩余物质的质量(m)与反应时间(t)的关系如图:
兴趣小组的同学们从山上采集到一种石灰石(主要成分为碳酸钙),他们将25克该样品放入盛有100g稀盐酸的烧杯中,恰好完全反应(杂质不与稀盐酸反应,也不溶于水),测得反应后烧杯中剩余物质的质量(m)与反应时间(t)的关系如图:| 100 |
| x |
| 44 |
| 8.8g |
| 20g |
| 25g |


 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
 ,从图中你获得的信息有(写二条即可)
,从图中你获得的信息有(写二条即可)
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
| 验实号编 | 试 剂 | 前 10min 内产生的氢气体积(mL) | |
| 不同纯度的锌 | 不同体积和浓度的稀硫酸 | ||
| a | 纯锌 | 30mL 30% | 564.3 |
| b | 含杂质的锌 | 30mL 30% | 634.7 |
| c | 纯锌 | 30mL 20% | 449.3 |
| d | 纯锌 | 40mL 30% | 602.8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com