
【题目】下图是一氧化碳与氢气在一定条件下发生化学变化的微观示意图(假设图示中的所有分子均参与化学反应)。通过比较、分析、归纳回答下列问题:
(1)一氧化碳分子与水分子的不同点是______________,相同点是___________。

(不利用相对原子质量)
(2)写出上述反应的化学方程式:___________。
(友情提示:甲物质的化学式请按照碳、氢、氧的顺序书写)。
(3)根据上述示意图,请你从微观角度描述你获得的关于化学变化的一条信息是________。
 优等生题库系列答案
优等生题库系列答案科目:初中化学 来源: 题型:
【题目】二氧化碳是我们熟悉的气体之一,是绿色植物进行光合作用的原料之一,小明同学查阅到的有关二氧化碳气体的资料如下:二氧化碳是一种没有颜色、没有气味的气体,密度比空气大;二氧化碳能使澄清石灰水变浑浊;点燃镁条,镁条在二氧化碳中燃烧,冒黑烟、发光、生成白色固体,生成了氧化镁和碳;二氧化碳可用作气体肥料、作制冷剂等.以上叙述中:
(1)属于二氧化碳的物理性质的是__________________________ 。
(2)二氧化碳的用途是 _____________________ 。(填的不全扣一分)
(3)镁条在二氧化碳中燃烧的化学方程式___________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】结合下列化学实验装置,回答有关问题。
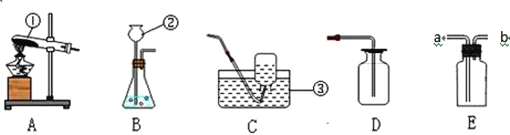
(1)写出带有标号②的仪器名称________ 。
(2)实验室用高锰酸钾制取氧气的符号表达式是 ______,其基本反应类型为 _______,用A做发生装置时,应作何改进_____。要收集较为纯净的氧气,应选择的收集装置为_________,利用该装置判断集气瓶内氧气是否收集满的依据是_______。若E中装满水,则收集氧气时气体应从________(a或b)端通入。
(3)硫化氢(H2S)气体是一种密度比空气大,能溶于水的有毒物质,其水溶液叫氢硫酸.实验室常用硫化亚铁(FeS)固体和稀硫酸溶液在常温下发生反应制取硫化氢气体,应选择的发生装置是_______,硫化氢可以燃烧,燃烧后生成一种有刺激性气味的气体和一种常见液体,请写出该反应的符号表达式_____,小虹同学认为收集硫化氢气体可用D或E装置,但小娟提出了质疑,小娟的理由是_______。
(4)为了测定空气中氧气含量, 小明小组设计了如图的装置进行探究活动。
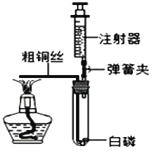
(步骤与现象)
①试管的容积为50mL;
②检查装置的气密性良好;
③装药品,将注射器活塞调整到合适位置,连接好仪器;
④弹簧夹夹紧胶皮管,加热粗铜丝,观察现象;
⑤燃烧结束,试管冷却到室温后打开弹簧夹,观察注射器活塞的移动情况。
(反思与交流)(1)兴趣小组同学测量试管容积的方法可能是________;
(2)小华同学认为步骤⑤在保证活塞自由移动的前提下,观察活塞位置时,最好将试管和注射器整体横放,小华同学的理由是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】过氧化氢在生产生活中有广泛应用,实验小组对过氧化氢进行探究。
(一)探究过氧化氢制取氧气
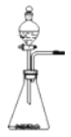
(1)分液漏斗中应放入的物质是_______,锥形瓶中应放入的物质是_______。写出该反应的符号达式__________________________,基本反应类型是_______。
(2)与高锰酸钾加热制取氧气相比,此法优点是_______(填编号)。
① 生成物只有氧气 ② 不需加热 ③ 更环保
(二)微观探究:如图是过氧化氢分解的微观示意图,据图回答:
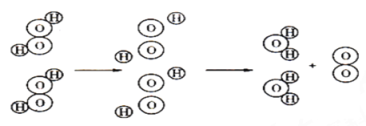
(3)一个过氧化氢分子由__________和____________构成。根据上图可以得出,在化学变化中__________可以再分,而________不能再分。
(三)不稳定性探究:探究温度对过氧化氢分解速率的影响。
晓晓为了探究温度对H2O2分解速率的影响,利用如图所示装置(夹持装置略去)进行实验(水浴是利用热水进行加热),实验数据如下表:
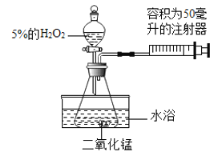
实验1 | 实验2 | |
MnO2的质量/克 | 0.5 | 0.5 |
5%的H2O2的体积/毫升 | 40 | X |
温度/℃ | 20 | 80 |
(4)实验2中X的值应为_______毫升。
(5)实验中可通过___________________________来比较H2O2分解速率的大小。
(6)实验2中水浴温度控制在80℃时,测定的反应速率会比真实值偏大,其原因是_______。
A.锥形瓶内气体受热膨胀 b.收集到的氧气中混有空气
C.温度较高时水蒸发成水蒸气 d.生成更多的氧气
(7)实验结束后若要将MnO2从混合物中分离出来,可采取的方法是_______、洗涤、干燥。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】空气是一种重要的自然资源。
(1)食物的腐败主要与空气中的______气体有关,为延长食品保质期,常常在食品包装袋中充入空气中含量最多的气体,该气体是__(填化学式)。
(2)氦气是一种稀有气体,其化学式为__,氦气可用于填充探空气球,这是利用它______的性质。与用氢气填充气球相比,用氦气填充气球的优点是______。
(3)下图是三种测定空气中氧气含量的装置图:
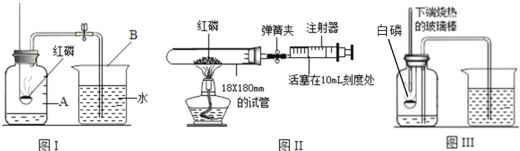
①图I实验中红磷燃烧的现象是______,反应的化学式表达式为______。
②图II实验中检查装置气密性的方法是______,试管的中空气的体积约为40毫升,燃烧红磷时弹簧夹处于关闭状态,等试管冷却打开弹簧夹,理论上注射器活塞最终应停留在刻度______mL处。
③图III实验过程中集气瓶中液面变化是______,与图I实验相比较,该实验具有的优点有______。
A.不需要将白磷在瓶外点燃再插入集气瓶,可以使测定结果更准确
B.白磷燃烧时,集气瓶中的水可以起到缓冲气压的作用
C.可以减少环境污染
(4)下图是是以空气和其他必要的原料合成氮肥碳酸氢铵(NH4HCO3)的流程.请按要求回答下列问题:
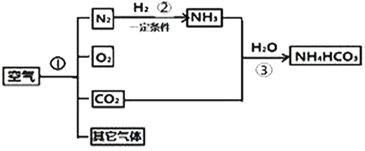
①步骤I可以根据液态氮和液态氧的______不同分离液态空气获得氮气和氧气,该过程属于______变化。
②写出步骤②中发生反应的化学式方程式______。
③据国家标准,碳酸氢铵化肥中纯碳酸氢铵的含量不得低于95%。可用将碳酸氢铵化肥与碱溶液反应,将其中氮元素全部转化为氨气来测定化肥中氮元素的含量(化肥中其他成分不含氮)。取某碳酸氢铵化肥样品8.0与足量碱溶液反应得到氨气的质量如下表所示:
试验次数 | 1 | 2 | 3 |
样品质量(g) | 8.00 | 8.00 | 8.00 |
氨气质量(g) | 1.71 | 1.69 | 1.70 |
通过以上数据计算该化肥中碳酸氢铵的含量是否达到国家标准。(写出计算过程,)______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】复习时,常用专题探究的方法学习常见物质的组成与性质,课堂上老师引导我们回顾了几个探究实验。
探究1:研究常见物质组成
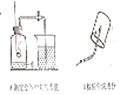
A和B都是研究物质组成的实验。从研究方法得知,A实验是利用可燃物消耗瓶内的____, 使瓶内压强减小来推测空气里氧气含量的: B实验是通过证明生成物的___________来推断甲烷的组成的。
探究2:研究常见物质性质
「资料]氢氧化钠的溶液能够吸收二氧化碳。
步骤1:烧杯中放入氢氧化钠溶液,燃烧匙中放入木炭,
点燃木炭后,迅速将燃烧匙伸入集气瓶,塞紧瓶塞。
步骤2:从注射器中推入适量过氧化氢溶液。实验装置如图所示,请你结合以上资料和实验步骤,回答问题:
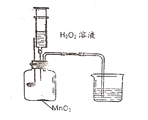
(1)写出木炭燃烧时发生反应的化学方程式:_________。
(2)推入H2O2溶液后,观察到木炭燃烧得更剧烈,由此得出氧气的化学性质是____,据此可知,木炭燃烧的剧烈程度与______有关。
(3)木炭熄灭后冷却一段时间,烧杯中的部分溶液流入集气瓶,请你结合该实验的反应原理分析集气瓶内压强的变化过程是__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学在学习中建构了“氮及其化合价的价、类关系图”。
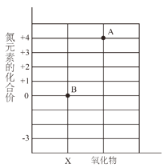
(1)图中A 点对应的物质为大气污染物之一,写出其对应的化学式:_____。
(2)写出图中B 点对应的物质化学式:_____,它对应的物质类别是:_____。
(3)浓氨水有挥发性,会挥发出氨气(NH3),标出 NH3 中氮元素化合价:_____。
(4)氮气的化学性质十分稳定,但在一定条件下能与氢气反应生成氨气。有 3g 氢气参加反应,理论上生成氨气的质量是多少?_____(请写出计算过程)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】二百多年前,法国化学家拉瓦锡用图1装置定量的研究了空气的成分。仿照这个历史上著名实验的原理,用图2所示装置来测定空气中氧气的含量。
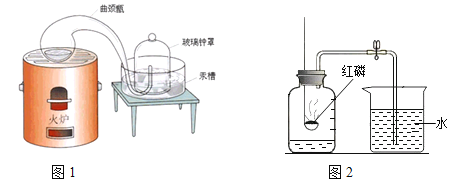
(实验回顾)图2是实验室用红磷燃烧来粗略测定空气中氧气含量的装置。写出红磷燃烧的符号表达式____。此实验不仅可以测定氧气占空气的体积分数,还可以说明氮气具有的化学性质是______(只需写一点)。
(分析讨论)用红磷燃烧的方法测出的氧气含量总是低于21%,有没有其他物质可以代替红磷进行实验而使实验结果更准确呢?
(实验改进1)同学们用蜡烛代替红磷测定空气中氧气的含量,发现蜡烛很快熄灭,回流到集气瓶中的水远远小于瓶中气体体积的1/5。是什么原因所致呢?
(猜想与假设)猜想①:蜡烛燃烧产生CO2气体;猜想②:__________。
(实验验证)将蜡烛点燃后用氧气传感器定量测定瓶中的氧气含量,数据如图3。

(得出结论)空气中氧气体积分数降低了______%。
(查阅资料)在老师的指导下,同学们查阅了红磷、白磷、蜡烛等可燃物燃烧所需要的最低含氧量以及其他信息如下:
资料1:
可燃物名称 | 红磷 | 白磷 | 蜡烛 |
最低含氧量/% | 8.0 | 4.0 | 16.0 |
甲、乙、丙三个小组分别用过量红磷、白磷、蜡烛进行该实验,用测氧气浓度的传感器测得反应后的氧气浓度分别为8.85%、3.21%、16.7%,数据与表中的理论值基本一致。其中蜡烛燃烧后用测一氧化碳浓度传感器测算一氧化碳浓度约为2%。
资料2:二氧化碳因与氢氧化钠溶液发生化学反应,实验室常用氢氧化钠溶液来吸收二氧化碳。
资料3:蜡烛或者木炭在密闭的集气瓶中燃烧,氧气浓度不断变小的同时,会有一氧化碳气体生成。常温下一氧化碳难溶于水,且不与氢氧化钠溶液反应。
(交流与讨论)根据以上信息回答下列问题:
①白磷和红磷相比,使用白磷能使结果更准确,其原因是__________。
②有同学提议选用木炭替代红磷做实验,在集气瓶底部预先放少量氢氧化钠溶液吸收生成的二氧化碳气体,小华觉得不可行,其主要原因是___________。
(实验改进2)食品脱氧剂(以铁粉为主的物质组成)能通过化学反应除去密闭包装袋中的氧气,使食品处于无氧状态。同学们尝试用图4装置进行实验来测定空气中氧气的含量。
下表是实验过程中记录的有关数据:
实验所需的时间/min | 0 | 5 | 10 | 30 | 35 | 45 |
量筒中液面的刻度/mL | 50 | 35 | 27.5 | 19.7 | 19.7 | 19.7 |
①脱氧剂发生复杂的化学反应,首先是铁粉与氧气、水反应生成氢氧化亚铁固体,写出该反应的符号表达式________。
②分析表中数据得知,至少经过________分钟后,量筒中的液面不再下降。
③根据表中实验数据进行推算,广口瓶中氧气的体积分数约为__________(结果精确到0.1%)
(实验拓展)铁在不同的条件下与氧气反应可生成不同种铁的氧化物, 58g四氧化三铁与多少克氧化铁(Fe2O3)中所含铁元素质量相等?_______(写出计算过程)
p>(实验评价)与燃烧红磷法相比,用脱氧剂测定空气中氧气含量的优点是__________。查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是元素周期表的一格,从中获取的信息不正确的是( )

A. 该元素属于金属元素
B. 该元素的原子在化学反应中易失去电子
C. 该元素位于第三周期
D. 该元素在地壳中质量分数为26.98%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com