
【题目】CaSO42H2O受热会逐步失去结晶水.取纯净的CaSO42H2O固体3.44g进行加热,测定固体质量随温度的变化情况如图所示.C点固体的化学式是_____.T3~T4温度段加热固体所产生的气体是形成酸雨的主要物质之一,则D~E段发生反应的化学方程式为_____.

科目:初中化学 来源: 题型:
【题目】如图为A、B、C三种物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )
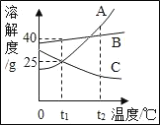
A. t1℃时,A、C两种物质饱和溶液中含有的溶质质量一定相同
B. t1℃时,A溶液溶质质量分数为20%
C. t2℃的三种物质的饱和溶液降温到t1℃时,溶质质量分数由大到小的顺序为B>A=C
D. t1℃时,125gA物质的饱和溶液加水稀释可以得到250g质量分数10%的A物质的溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
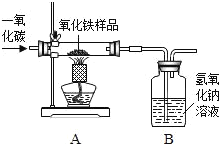
【题目】现有一种不纯的氧化铁粉末样品(杂质为铁粉),小刚和小强通过实验测定样品中氧化铁的质量分数.请你回答相关问题:
(1)小刚称取10g样品,利用如图所示装置进行实验,相关实验数据见下表:(玻璃管内的物质完全反应)
编号 | 称量物 | 反应前 | 反应后 |
一 | 硬质玻璃管及所盛固体总质量 | 76.2g | 73.8g |
二 | B装置总质量 | 153.7g | 160.3g |
①由上表的数据可分析出,反应后硬质玻璃管及所盛固体总质量减少的是_____的质量.
②请根据B装置总质量变化的数据,计算出样品中氧化铁的质量分数_____(写出计算过程).
(2)为达到同样的实验目的,小强设计的方案为:将一定质量的样品于过量的稀盐酸反应,准确称量反应前、后固体和液体物质的总质量,据此可求出氧化铁的质量分数.
请你分别对小刚和小强设计的实验方案进行评价(各写出一条即可):_____.
(3)如果小强还想计算出所用稀盐酸的溶质质量分数,请简要说明对其方案的改进方法及原因:_____;_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小华同学在复习酸碱盐知识时整理了如下网络图,“→”表示相互转化,“—”相互反应。已知A、B、C、D是初中化学常见的物质,为金属单质、金属氧化物、碱和盐中的各一种,下列说法不正确的是
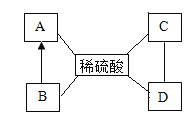
A. 如果A是铁,则A与稀硫酸反应产生气泡,溶液变成浅绿色
B. 如果B是金属氧化物,B转化为A可能是工业炼铁的原理
C. 如果C溶液呈碱性,则D只能是盐
D. 如果D与稀硫酸反应产生二氧化碳,则C只能是碱
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)要组装出实验室用高锰酸钾受热分解制氧气的发生装置,应选择下列仪器中的______(填序号)。反应的化学方程式是____。
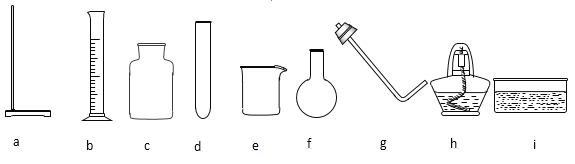
(2)实验室还可用下图的装置制取氧气。该反应的化学方程式是_____;此装置中烧瓶可用上图所给仪器中的____替代(填序号)。该装置还可用于制取的气体是___。
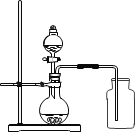
(3)若用如图的装置经过较长时间仍没有收集满一瓶气体,请分析可能的原因___(写一条即可)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硅钢可用于制造变压器的铁芯,某化学兴趣小组的同学为了验证硅钢(主要含有Fe、C、Si),设计了如图的试验流程(有些反应的部分反应物和生成物已省略).查阅资料发现常温下,单质硅(Si)不能与盐酸反应,但能与氢氧化钠溶液反应(Si+2NaOH+H2O═Na2SiO2+2H2↑).

根据以上信息,回答下列问题:
(1)固体A的成分为 ,滤液B中的金属阳离子为 ;
(2)写出步骤⑦中发生反应的化学方程式 ;其基本反应类型为 ;
(3)在过滤操作时,若发现滤液浑浊,应 ;
(4)步骤⑤中发生的是化合反应,尝试写出其化学方程式 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】食盐、碳酸钠和碳酸氢钠是生活中常见的钠盐。请回答下列问题。
(1)碳酸氢钠的水溶液显_____性(填“酸”、“碱”或“中”)。碳酸氢钙受热易分解,碳酸氢钠性质与其相似,除去碳酸钠固体中混有的少量碳酸氢钠,反应的化学方程式为_______________________________。
(2)等质量的碳酸钠和碳酸氢钠分别与足量盐酸反应时生成的CO2量,前者_____后者(填“>”、“<”或“=”)。
(3)粗盐含有少量杂质(主要为CaCl2、MgCl2、Na2SO4等)。用粗盐制取“化学纯”级的NaCl,步骤为溶解、加过量a、加过量NaOH、加过量b、过滤、加适量盐酸,蒸发结晶得到“化学纯”级的NaCl固体。试剂a、b分别是_____(填序号)
A Na2CO3、BaCl2 B BaCl2、Na2CO3 C BaCl2、Na2SO4
(4)工业上用电解饱和食盐水的方法生成氯气和烧碱。
资料一:Cl2+H2O=HCl+HClO
资料二:初中化学中,我们学习了酸和碱发生中和反应的实质是H++OH﹣=H2O,像这种用实际参加反应的离子符号来表示反应的式子叫离子反应,离子方程式的书写一般按以下步骤:(以Na2SO4与BaCl2反应为例)
①写出Na2SO4与BaCl2反应的化学方程式:_________________________
②把易溶于水,易电解的物质写成离子形式,把难溶的物质、气体和水等仍用化学式表示,上述化学方程式可改写成,2Na++SO42﹣+Ba2++2Cl﹣=BaSO4↓+2Na++2Cl﹣
③删去方程两边不参加反应的离子:Ba2++SO42﹣=BaSO4↓:
④检查方程式两边各元素的原子个数和电荷总数是否相等
⑤某化工厂发生氯气泄漏事件,工作人员喷射NaOH溶液形成液幕,包围并吸收泄漏的氯气,其反应原理________________________(用离子方程式表示)
资料三:化学反应类型有不同的分法,其中反应前后,有元素化合价变化的化学反应是氧化还原反应。氧化还原反应中有元素化合价升高的反应物是还原剂,有元素化合价降低的反应物是氧化剂,化合价没有发生变化的既不是氧化剂也不是还原剂。
⑥工业上可用氨检验输送氯气的管道是否漏气。反应方程式如下:8NH3+3Cl2=6NH4Cl+N2,该反应_____(填“是”或“不是”)氧化还原反应,其中氧化剂和还原剂物质的量之比为__________(若是氧化还原反应,此空作答,反之,不作答)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图中A、B、C、D是四种粒子的结构示意图.

请回答下列问题:
(1)图中A、B、C、D属于_____种元素的粒子.
(2)A、B、C、D四种粒子中,不具备稳定结构的是_____(填序号),它在化学变化中容易_____(填“得到”或“失去”)电子,成为离子.
(3)D中x=_____.
(4)A与C形成化合物的化学式是_____.
(5)B单质在氧气中燃烧的化学方程式_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】味精是主要成分谷氨酸钠,易溶于水,其化学式是C5H8NO4Na,与硝酸银溶液不反应。味精中还含有氯化钠(味精中其他成分不考虑),氯化钠与硝酸银溶液发生复分解反应,生产氯化银白色沉淀。回答下列问题:
(1)称取5.0g味精配制成50g溶液,量取蒸馏水的量筒规格是________(填字母)。
A.10mL B.50mL C.100 mL
(2)如图是配制过程,正确的操作顺序为________((填序号)。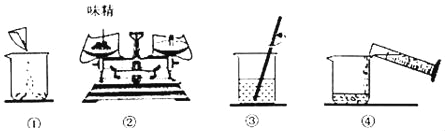
(3)为测定味精中NaCl的质量分数,进行如下实验:
在其他操作均正确的情况下,若在配制溶液过程中,仰视刻度量取蒸馏水,则所配制溶液的谷氨酸钠质量分数________((填“偏大”、“偏小”或“无影响”)
(4)为测定味精中含有氯化钠的质量分数,继续实验:
①向所配制的50g溶液中加入过量的________(溶液(填化学式)充分反应。
②然后进行________((填操作名称)、洗涤、干燥、称量白色沉淀固体。经精确测定白色沉淀的质量为2.87g,则该味精中氯化钠的质量分数为_________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com