
 农作物缺少氮元素时,就需要向田里施入含有氮元素的肥料,通过计算判断该化工厂的广告是真的还是假的?
农作物缺少氮元素时,就需要向田里施入含有氮元素的肥料,通过计算判断该化工厂的广告是真的还是假的? 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
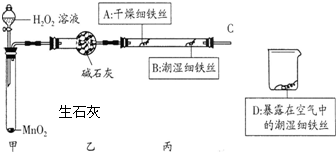
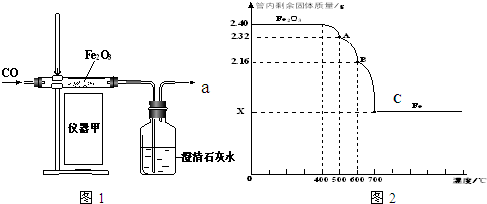
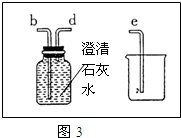
| 实验方案 | 实验现象 |
| 分别取少量A、B、C点固体用磁铁感应,然后加入硫酸铜溶液中 | A点固体可被磁铁感应,硫酸铜溶液中无任何现象 |
| B点固体不可被磁铁感应,硫酸铜溶液中无任何现象 | |
| C点固体可被磁铁感应,硫酸铜溶液中有红色固体出现 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:

| 实验步骤 | 实验现象 | 实验结论 |
| ①取等体积的两种液体于A、B两个试管中. ②分别向A、B两试管中加入等质量(少量)的 | A试管中无明显现象 B试管中的现象是 | 结论是 涉及的化学反应式是 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com