
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写即可.
解答 解:碳酸氢钙受热会生成碳酸钙水与二氧化碳,反应的化学方程式为:Ca(HCO3)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCO3↓+CO2↑+H2O;
水垢成分是CaCO3和Mg(OH)2,碳酸钙与醋酸反应生成醋酸钙、水和二氧化碳,氢氧化镁与醋酸反应生成醋酸镁和水,反应的化学方程式分别是CaCO3+2CH3COOH=Ca(CH3COO)2+H2O+CO2↑、Mg(OH)2+2CH3COOH═Mg(CH3COO)2+2H2O;
故答案为:Ca(HCO3)$\frac{\underline{\;\;△\;\;}}{\;}$CaCO3+H2O+CO2↑
CaCO3+2CH3COOH=Ca(CH3COO)2+H2O+CO2↑
Mg(OH)2+2CH3COOH=Mg(CH3COO)2+2H2O
点评 此题是一道生活实际的考查题,解题的关键是对化学与生活实际的联系的掌握和化学方程式的正确书写,属基础性知识考查题.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 9:15:5 | B. | 9:20:13 | C. | 5:7:13 | D. | 5:9:15 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 2:3 | B. | 3:2 | C. | 2:1 | D. | 1:2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 滤渣中必定含有Zn、Cu,可能含有Fe | |
| B. | 滤渣中必定含有Fe、Zn,可能含有Cu | |
| C. | 滤液中必定含有Zn2+,可能含有Fe2+ | |
| D. | 滤液中必定含有Zn2+、Fe2+,可能含有Cu2+ |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
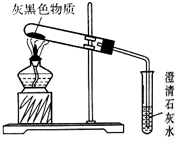 镁是一种银白色的金属,但实验室看到的镁条常常有一层灰黑色的“外衣”,这层灰黑色的外衣是什么物质呢?甲同学认为是MgO;乙同学认为是Mg2(OH)2CO3;丙同学认为是Mg(OH)2.
镁是一种银白色的金属,但实验室看到的镁条常常有一层灰黑色的“外衣”,这层灰黑色的外衣是什么物质呢?甲同学认为是MgO;乙同学认为是Mg2(OH)2CO3;丙同学认为是Mg(OH)2.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验操作 | 实验现象 | 实验结论 |
| 取少量固体剩余物于试管中,向其中加入足量的稀盐酸. | (1)固体部分溶解,溶液为无色. | 假设①成立.[来 |
| (2)固体部分溶解,有气体生成,溶液为无色. | 假设②成立. | |
| (3)固体部分溶解,溶液为蓝色. | 假设③成立. |
| 实验组别 | I | II | III | IV | V |
| 药 品 | Al | Fe | Ag | Al | Cu |
| CuO | CuO | CuO | Fe2O3 | Fe2O3 | |
| 相同条件下是否反应 | 是 | 是 | 否 | 是 | 否 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com