
| 次数 | 1 | 2 | 3 | 4 |
| 加入稀硫酸质量/g | 70.0 | 70.0 | 70.0 | 70.0 |
| 剩余固体质量/g | 13.6 | 11.2 | 8.8 | 8.4 |
分析 根据反应物、生成物、反应条件及其质量守恒定律可以书写反应的化学方程式;
显碱性的溶液能使酚酞试液变红色,显中性或显酸性的溶液不能使酚酞试液变色;
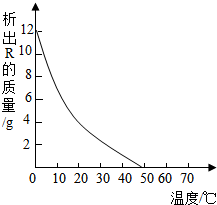
氢氧化镁的溶解度随着温度的降低而减小;
溶解的氢氧化镁能和二氧化碳反应生成碳酸镁沉淀和水;
通过对比可以判断推测是否正确.
(5)①混合物粉末中铜的质量分数=$\frac{铜的质量}{混合物粉末质量}$×100%需要求出铜的质量;铜不能与酸发生置换反应,因此,当金属混合物粉末与足量稀硫酸完全反应后,剩余固体质量即为铜的质量;
②由于70克硫酸参加反应金属减少2.4克,由此可以求出第四次参加反应硫酸的质量,根据参加反应金属的质量与参加反应硫酸的质量计算金属的相对原子质量;根据相对原子质量判断金属元素;
③第三次加入硫酸充分反应后,由于金属有剩余因而所加稀硫酸完全反应,所得溶液为金属的硫酸盐溶液;根据反应的化学方程式则消耗金属的质量计算出反应生成硫酸盐的质量,所得质量与溶液的质量比即得溶液的质量分数;反应后所得溶液的质量由质量守恒定律进行求得.
解答 解:(1)金属镁与热水反应的化学方程式为:Mg+2H2O(热)=Mg(OH)2+H2↑.
故填:Mg+2H2O(热)=Mg(OH)2+H2↑.
(2)溶液的红色褪去说明溶液的碱性消失.
故填:消失.
(3)①导致溶液碱性变化的原因可能是:氢氧化镁的溶解度随着温度的降低而减小,从而使溶液碱性消失;
②也可能是:吸收了空气中的二氧化碳而使溶液碱性消失.
故填:①氢氧化镁的溶解度随着温度的降低而减小,从而使溶液碱性消失;②吸收了空气中的二氧化碳而使溶液碱性消失.
(4)实验操作:取上述等量的红色溶液分别与空气接触和隔绝空气的条件下冷却;
实验现象:与空气接触的酚酞试液不褪色,隔绝空气的条件下冷却的酚酞试液褪色;
实验结论:导致溶液碱性变化的原因是氢氧化镁的溶解度随着温度的降低而减小,从而导致溶液的碱性消失.
(5)①该粉末中Cu的质量分数为$\frac{8.4g}{16g}$×100%=52.5%;
(2)设:另一种金属为M,其相对分子质量为x
分析表格中数据可知每70g稀硫酸与2.4g金属M恰好完全反应
M+H2SO4═MSO4 +H2↑
x 98
2.4g 70g×14%
$\frac{x}{2.4g}=\frac{98}{70g×14%}$
x=24
该金属为镁;
(3)第3次加入稀硫酸充分反应后,消耗金属镁的质量为7.2g.
设:此时生成MgSO4的质量为y,生成 H2的质量为z
Mg+H2SO4═MgSO4 +H2↑
24 120 2
7.2g y z
$\frac{24}{7.2g}=\frac{120}{y}=\frac{2}{z}$
y=36g
z=0.6 g
则此时所得溶液中溶质质量分数为$\frac{36g}{7.2g+3×70g-0.6g}×100%$=16.6%;
答:(1)该粉末中Cu的质量分数为52.5%;
(2)该粉末中另一种金属为镁;
(3)第3次加入稀硫酸充分反应后,所得溶液中溶质的质量分数为16.6%.
点评 本题考查内容较多,合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,根据质量守恒定律,第三次加入稀硫酸充分反应后所得溶液的质量=参加反应金属的质量+三次所加稀硫酸的质量-反应放出氢气的质量;利用根据守恒定律化复杂的溶液计算为简便明了.


科目:初中化学 来源: 题型:解答题
 溶液在生产和科研中具有广泛的用途,与人们的生活密不可分.
溶液在生产和科研中具有广泛的用途,与人们的生活密不可分.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 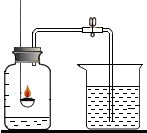 该实验是利用可燃物燃烧,放出热量,使瓶内气体膨胀来测定空气中氧气的含量 | |
| B. | 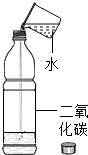 该实验中观察到塑料瓶变瘪,说明二氧化碳能溶于水 | |
| C. | 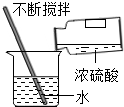 该实验中玻璃棒的作用是搅拌,加快浓硫酸的溶解 | |
| D. | 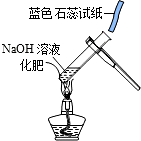 该实验可用于检验铵态氮肥 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | 所含杂质 | 除去杂质的试剂或方法 | |
| A | 02 | N2 | 通过灼热的铜网 |
| B | CO2 | HCl | 通过足量的氢氧化钠浓溶液 |
| C | CaO | CaCO3 | 高温煅烧 |
| D | NaCl | KCl | 加入足量的硝酸银溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
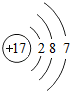 已知如图为某粒子的结构示意图,下列说法正确的是( )
已知如图为某粒子的结构示意图,下列说法正确的是( )| A. | 该元素位于第三周期 | |
| B. | 该元素在化合物中常显+1价 | |
| C. | 该元素的一个离子含有17个电子 | |
| D. | 该元素的原子在化学反应中容易失去电子 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 镁在氧气中燃烧:4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 | |
| B. | 用电解水的方法测定水的组成2H20=2H2↑+O2↑ | |
| C. | 在密闭容器中燃烧白磷验证质量守恒定律4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5 | |
| D. | 用稀硫酸清洗试管内壁附着的铜Cu+H2SO4=CuSO4+H2↑ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 智能手机耗电量大,移动充电宝应运而生,如图是一款应充电宝的示意图.
智能手机耗电量大,移动充电宝应运而生,如图是一款应充电宝的示意图.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com