
 水是生命之源,扬州是运河之城,也是南水北调的起点.请根据题意回答下列有关水溶液的问题.
水是生命之源,扬州是运河之城,也是南水北调的起点.请根据题意回答下列有关水溶液的问题.分析 (一)据溶质的质量分数=$\frac{溶质质量}{溶质质量+溶剂质量}$×100%分析解答;
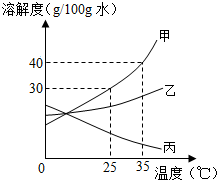
(二)(1)据该温度下甲的溶解度分析解答;
(2)不饱和溶液变为饱和溶液的一般方法是加入溶质、蒸发溶剂;
(3)据甲乙的溶解度受温度影响情况分析提纯物质的方法;
(4)丙的溶解度随温度升高而减小,据此分析解答;
(5)向100g35℃的水中加入48g甲固体,发现全部溶解,一段时间后又有部分甲的晶体析出,可能是甲溶解时放热,使溶解度增大.
解答 解:(一)将10克NaOH固体完全溶解在40毫升水中,水的质量是40g,所配溶液中溶质的质量分数为$\frac{10g}{10g+40g}$×100%=20%.某同学在配制过程中,量取水时仰视读数,则所取的水的体积偏大,其所配氢氧化钠溶液中溶质的质量分数将偏小;另一位同学称取NaOH时,由于操作不熟练,花了较长时间,氢氧化钠会吸水且与二氧化碳反应,导致溶质变少,溶剂变多,他所配氢氧化钠溶液中溶质的质量分数将偏小.
(二)(1)25℃时,甲的溶解度为30g,将25g甲固体加入到50g水中,充分溶解并恢复到原温度后,只能溶解15g,得到溶液的质量为15g+50g=65g.
(2)要使35℃时接近饱和的甲溶液变成该温度下的饱和溶液,可采用蒸发水或是加入甲物质.
(3)甲的溶解度受温度影响变化大,故若甲固体中含有少量乙,提纯甲的操作步骤是先溶解、加热浓缩、然后降温结晶、过滤.
(4)将35℃时丙的饱和溶液降温到25℃,丙的溶解度随温度的降低而增大,故溶液的组成不变,则其溶液的溶质质量分数不变.
(5)向100g35℃的水中加入48g甲固体,发现全部溶解,一段时间后又有部分甲的晶体析出.你认为“全部溶解”的原因可能是 甲溶解时放热,溶液度增大.
故答案为:(一)20%; 偏小; 偏小;
(二)(1)65g; (2)加入甲物质(或蒸发少量水); (3)adcb; (4)不变;(5)甲溶解时放热,溶液度增大.
点评 本题考查的是溶液的配制以及溶解度曲线的应用的知识,完成此题,可以依据已有的知识进行.


科目:初中化学 来源: 题型:选择题
| A. | 尽可能用太阳能热水器代替燃气热水器 | |
| B. | 将废电池和生活垃圾一起丢进垃圾箱 | |
| C. | 在旱地上进行大规模的农牧业生产活动 | |
| D. | 将工业的废水和生活的污水大量排入江河湖泊 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 2014年,黑龙江省的粮食产量又跃居全国第一,如图是某农场的一块麦田,请回答有关问题:
2014年,黑龙江省的粮食产量又跃居全国第一,如图是某农场的一块麦田,请回答有关问题:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
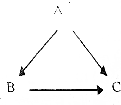 初中化学学习存在许多“二角”关系.A、B、C都是初中常见的物质,其转化关系如图所示.
初中化学学习存在许多“二角”关系.A、B、C都是初中常见的物质,其转化关系如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氧气的分子结构与新型“氧分子”的结构应该相同 | |
| B. | 氧气的分子结构与新型“氧分子”的物理性质应该不同 | |
| C. | 新型“氧分子”与氧分子都是由氧原子构成的 | |
| D. | 每个新型氧分子与每个氧气分子含有的氧原子数不同 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 涤纶、羊毛和棉花都是天然纤维 | |
| B. | 各种塑料在自然界都不能降解 | |
| C. | 电木插座破裂后可以热修补 | |
| D. | 合成橡胶有高弹性、绝缘性等优良性能 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
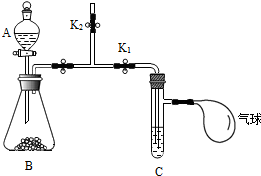 实验:研究CO2与NaOH固体的反应
实验:研究CO2与NaOH固体的反应查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com