
【题目】为了探究石灰石与稀盐酸反应制备二氧化碳后的废液中的溶质成分,将废液过滤,取滤液224.4克于烧杯中,在不断振荡的条件下,向其中逐滴加质量分数为10.6%的碳酸钠溶液直至过量,有关的变化如图所示。经测定A中只含有一种溶质。根据题中有关信息和图像分析回答下列问题。
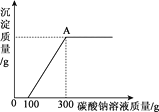
(1)原废液中的溶质成分有________(用化学式回答)
(2)该碳酸钠溶液中钠元素的质量分数为_________(结果保留到0.1%)
(3)A点处溶液中溶质的质量分数是多少?(列出必要的解题步骤,结果保留到0.1%)
【答案】(1)CaCl2,HCl;(2)4.6%;(3)6.1%
【解析】由题中信息知,(1)原废液中的溶质成分有CaCl2,HCl;
(2)碳酸钠相对分子质量是106,Na2CO3→2 Na.106→46,该碳酸钠溶液中钠元素的质量分数为4.6%;(3)A点处溶液中溶质的质量分数是∶
Na2CO3+2HCl=2NaCl+CO2 ↑+H2O
106 117 44
100g×10.6% x z
![]() =
=![]() ,x=11.7g.
,x=11.7g. ![]() =
=![]() ,z=4.4g.
,z=4.4g.
Na2CO3+CaCl2=Ca2CO3 ↓+2NaCl
106 100 117
200g× 10.6% z y
![]() =
= ![]() ,y=23.4g .
,y=23.4g . ![]() =
= ![]() ,z=20g.
,z=20g.
A点处溶液中溶质的质量分数是∶![]() ×100%=6.1%.
×100%=6.1%.
答∶ (1)原废液中的溶质成分有CaCl2,HCl;
(2)该碳酸钠溶液中钠元素的质量分数为4.6%;
(3)A点处溶液中溶质的质量分数是6.1%.
点睛∶本题主要考查质量守恒定律的应用以及根据化学方程式进行计算。


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
【题目】归纳、分类、比较、推理是学习化学常用的方法。现有A~F六种物质,均是由H、C、N、O、Cl、Na、Ca中的两种或三种元素组成。请回答下列问题:
(1)上述七种元素中属于金属元素的是________(填元素名称)。
(2)A属于氧化物,是导致酸雨的气体污染物之一,组成A的两种元素的质量比为7∶8,则A的化学式为____________。
(3)B、C常温下均为液体,且组成元素相同,B在一定条件下可生成C,写出该反应的化学反应方程式_______________________________________。
(4)D用于玻璃、造纸、纺织和洗涤剂的生产,E、F均由两种元素组成,取D溶液进行实验,操作和现象如下图:
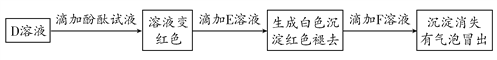
写出D与E反应的化学方程式_________,F的化学式为____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A~E是初中化学中常见的物质,下图为这些物质的相互转化关系图,图中“—”表示相连的物质间能相互发生反应,“→”表示物质间有相应的转化关系。其中,A、B都是黑色固体,通常状况下,C是一种能使澄清石灰水变浑浊的气体,D溶于水形成蓝色溶液,常用于配制一种具有杀菌作用的农药。请写出:

(1)物质C的化学式为_________;
(2)反应①的化学方程式为_______________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是固体物质M的溶解度曲线,下列说法正确的是

A. 40℃时,其饱和溶液中溶质的质量分数为50%
B. M的溶解度随温度升高而一直增大
C. 将40℃是M的饱和溶液降温至10℃,有固体析出
D. 将50℃时M的饱和溶液升温至80℃,溶液变为不饱和溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请结合下图中的A—F回答问题:
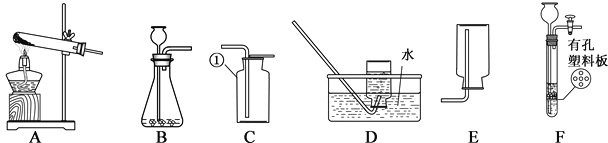
(1)标号①的仪器名称:__________。
(2)B与D组合可完成实验室制取H2气体的操作,其化学反应方程式为___________________________,若用F装置代替B装置,其优点是____________________________________________________________。
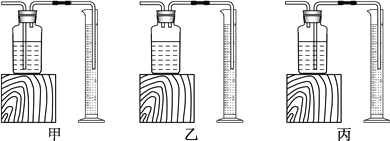
(3)实验室选用两种固体物质的混合物制氧气,则化学反应方程式是_______________________________,小松同学利用下图中________(选填“甲”、“乙”或“丙”)来收集并测定氧气的体积。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是固体物质a、b、c的溶解度曲线。下列说法正确的是

A. t1 ℃时,a、b、c溶解度的大小顺序是:a>b>c
B. t2 ℃时,a、b饱和溶液中溶质质量分数相等
C. t2 ℃时,将40 g 的c加到100 g水中,制得的溶液不饱和
D. 欲使c从溶液中结晶,可以采用降温结晶或蒸发溶剂的方法
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学兴趣小组在李老师指导下,改进了“测量空气中氧气体积分数”的实验装置(见下图),并进行以下实验探究活动,请你一同参与。
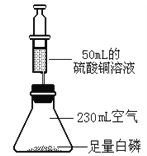
【查阅资料】
①白磷剧毒,着火点低(40℃),易燃烧,且耗氧彻底。
②硫酸铜溶液能与白磷反应,从而化解白磷的毒性。
【实验探究】
(1)在确保装置不漏气时,按图装入药品、连好仪器。
(2)将锥形瓶底部放入热水中,白磷很快被引燃。白磷燃烧的化学方程式是______。
(3)燃烧结束后,等到锥形瓶冷却到室温,按下注射器,使注射器针头穿透橡皮塞,此时注射器里的硫酸铜溶液会______,以弥补氧气的体积。如果实验比较成功,测得氧气的体积分数约是______,最终注射器里的液面约停留在______mL刻度处。
【反思评价】
(1)实验结束、振荡锥形瓶,硫酸铜溶液能与剩余的白磷发生反应,有关的化学方程式为:
11Px + 60CuSO4 + 96H2O = 20Cu3P↓ + 24H3PO4 + 60H2SO4,则x=_____。
(2)此改进装置与课本上“测量空气中氧气体积分数”实验装置相比,有不少的优点,请你写出1条:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】民族英雄于谦的石灰吟:“千锤万凿出深山,烈火焚烧若等闲。粉身碎骨浑不怕,要留清白在人间。”请你从化学的视角,找出符合诗句中物质变化顺序的选项
A.CaCO3→Ca(OH)2→CaO→CaCO3 B.CaCO3→CaO→Ca(OH)2→CaCO3
C.CaCO3→Ca(OH)2→CaCl2→CaCO3 D.Ca(OH)2→CaCO3→CaO→CaCO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com