
分析 (1)物理性质是指物质不需要发生化学变化就表现出来的性质;
(2)根据反应原理以及化学方程式的书写方法考虑;
(3)根据反应物的状态和硫化氢气体的密度和溶解性考虑;
(4)根据反应原理以及化学方程式的书写方法考虑;
(5)根据反应原理以及化学方程式的书写方法考虑.
解答 解:(1)物质的颜色、状态、气味、熔点、沸点、硬度、密度等性质,不需要发生化学变化就表现出来,因此,都属于物理性质,硫化氢(H2S)是一种无色且有臭鸡蛋味的气体属于颜色、气味、状态,密度比空气大属于密度,能溶于水属于溶解性,都属于物理性质;故填:无色、有臭鸡蛋味的气体、密度比空气大、能溶于水.
(2)反应物是硫化亚铁(FeS)与稀硫酸(H2SO4)生成物是H2S气体和FeSO4;故填:FeS+H2SO4=FeSO4+H2S↑;
(3)硫化亚铁(FeS)属于固体,稀硫酸属于液体,所以不需要加热;硫化氢气体密度比空气大,用向上排空气法收集,能溶于水不能用排水法收集;故填:固液不加热;向上排空气;
(4)硫化氢燃烧的反应物是硫化氢和氧气,生成物是硫和水,反应条件是点燃;故填:2H2S+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O+2S↓;
(5)当氧气充足时硫化氢燃烧的反应物是硫化氢和氧气,生成物是二氧化硫和水,用观察法配平,反应条件是点燃.故填:2H2S+3O2$\frac{\underline{\;点燃\;}}{\;}$2H2O+2SO2.
点评 答本题关键是要知道物理性质、化学性质是一对与物理变化、化学变化有密切关系的概念,联系物理变化、化学变化来理解物理性质和化学性质,则掌握起来并不困难;熟悉化学方程式的书写方法.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 将活性炭放入红墨水中,红墨水褪色 | |
| B. | 硫在空气中燃烧产生蓝紫色火焰 | |
| C. | 用稀盐酸除铁锈后溶液变成黄色 | |
| D. | 铜绿加热后固体变成黑 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 水是由氢、氧两种元素组成的化合物 | |
| B. | 在化学变化中,分子可分而原子不可分 | |
| C. | 化学反应前后,元素的种类不变 | |
| D. | 分子不停地运动,且分子之间有间隔 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
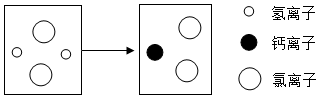
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O | B. | CO2+Ca(OH)2=CaCO3↓+H2O | ||
| C. | Mg+O2$\frac{\underline{\;点燃\;}}{\;}$MgO2 | D. | 3Fe+2O2=Fe3O4 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
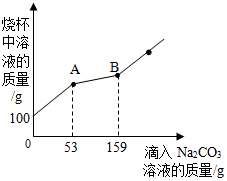 在一烧杯中盛有BaCl2和HCl的混合溶液,向其中逐渐滴加溶质质量分数为10%的Na2CO3溶液,混合溶液的质量与所滴入Na2CO3溶液的质量关系曲线如图所示,请根据题意问答问题:
在一烧杯中盛有BaCl2和HCl的混合溶液,向其中逐渐滴加溶质质量分数为10%的Na2CO3溶液,混合溶液的质量与所滴入Na2CO3溶液的质量关系曲线如图所示,请根据题意问答问题:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com