
【题目】A、B、C是三种常见的含钙化合物。它们之间有如图所示的转化关系(部分产物略去)。
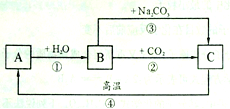
(1)A物质的化学式是 ,B物质的俗称是 ,C物质的名称是 。
(2)向A的块状固体上滴加水,观察到大量的水蒸气产生,该现象说明 。
(3)举出B物质在农业生产中的一种用途: 。
(4)反应②的化学方程式是 。该反应可用来检验二氧化碳气体,实验现象是 。
(5)反应③的基本反应类型是 ,该反应前后元素的化合价 (填“改变”或“不改变”)。
【答案】(1)CaO,熟石灰(消石灰),碳酸钙。(2)CaO与水反应放热。(3)用途:中和酸性土壤。
(4)反应②的化学方程式是Ca(OH)2+CO2=CaCO3↓+H2O。实验现象是生成白色沉淀。
(5)基本反应类型是复分解反应,元素的化合价不改变(填“改变”或“不改变”)。
【解析】
试题分析:根据图中转化关系可知,A能与水反应生成B,B与二氧化碳反应生成C,可以推知A是氧化钙,B是氢氧化钙,C是碳酸钙。(1)A物质的化学式是CaO,B物质的俗称是熟石灰(消石灰),C物质的名称是碳酸钙。(2)向A的块状固体上滴加水,观察到大量的水蒸气产生,该现象说明CaO与水反应放热。(3)熟石灰在农业生产中的一种用途是:中和酸性土壤。(4)反应②的化学方程式是Ca(OH) 2 + CO2 = CaCO3↓+ H2O。该反应可用来检验二氧化碳气体,将二氧化碳气体通入澄清石灰水中,石灰水变浑浊,即生成白色沉淀。(5)反应③是Ca(OH) 2 + Na2CO3 = CaCO3↓+ 2NaOH,该反应属于复分解反应,反应前后元素的化合价没有改变。


科目:初中化学 来源: 题型:
【题目】原电池中若用活泼性不同的两种金属作电极时,一般活泼性较强的作负极。现有A、B、C、D四种金属,只有A、C可与稀硫酸反应放出H2且A、C形成原电池时C作负极,D与B的硝酸盐溶液反应可置换出B的单质,则四种金属活泼性由弱到强的顺序是
A.A、C、D、B B.A、B、C、D
C.B、D、A、C D.C、A、D、B
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请根据图7中A、B两种固体物质的溶解度曲线,回答下列问题。

(l)在____℃时,A、B两种物质溶解度相同。
(2)t2℃时,100g水中溶解_ gA物质恰好达到饱和,该饱和溶液中溶质的质量分数为_ ___,若要把该饱和溶液稀释成质量分数为10%的溶液,应加水 _ ___g。
(3)将t2℃时A、B两种物质的饱和溶液降温至t1℃(其它条件不变),溶质的质量分数保持不变的是__ _。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业上用电解饱和NaCl溶液的方法来制取NaOH、Cl2和H2,并以它们为原料生产一
系列化工产品,称为氯碱工业。在工业上,制取氯气和烧碱的主要工艺流程如下:

环节Ⅰ:利用海水提取粗盐的过程(如图)。

(1)图中①是 (填“蒸发”或“冷却”)池。
(2)母液为氯化钠的 (填“饱和”或“不饱和”)溶液。
环节Ⅱ:利用工业上粗盐(含MgCl2、CaCl2、Na2SO4等杂质)精制氯化钠(工艺流程如下图)。

(1)X中含有的阳离子是 ;
(2)写出生成沉淀D的一个化学方程式 。
(3)溶液E中加过量稀盐酸的作用是 。
(4)实验所得精盐的质量大于粗盐中NaCl的质量,原因是 。
环节Ⅲ:电解饱和食盐水生产氯气和烧碱并测定烧碱的纯度。
(1)请写出环节Ⅲ生产中发生反应的化学方程式 。
(2)工业烧碱常常含有一定的氯化钠和碳酸钠杂质。为了测定烧碱的含量,小婉同学设计探究方案后进行实验并测得数据如图:

你利用小婉同学测得的数据计算烧碱样品中氢氧化钠的质量分数(请列出计算过程) 。
(3)小强同学认为小婉同学设计的探究方案不够严密,其理由是:
①探究方案中没考虑氢氧化钠的吸水性。
②探究方案中因缺少 (填操作名称),导致测得的氢氧化钠的质量分数偏小。
环节Ⅳ:应用举例
氯气与氢氧化钠溶液反应的化学方程式为:Cl2+2NaOH=NaCl+NaClO+H2O,工业上用氯气与石灰乳[Ca(OH)2]反应来制取漂白粉,有关反应的化学方程式是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】空气是一种宝贵的自然资源。下列对空气的说法中正确的是( )
A.空气中含量最多的是氧气,氧气可支持燃烧
B.空气中PM2.5含量高说明空气质量好
C.二氧化碳约占空气体积的0.03%,过多能产生温室效应,是一种空气污染物
D.臭氧分布在距地表15-25km的高空中,是一种空气污染物,在空气质量日报中被计入空气污染指数项目
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】利用中和反应可以测定酸或碱溶液中溶质的质量分数。例如,在一定量的待测酸(或碱)溶液中逐滴加入已知质量分数的碱(或酸)溶液(标准溶液),直到酸、碱正好完全反应,根据消耗标准碱(或酸)溶液的多少即可求算出待测酸(或碱)溶液的质量分数。 右图为某次测定过程中,溶液的pH随所滴加的...某标准溶液体积的变化而变化的关系图。
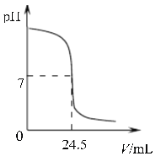
(1)根据右图曲线可以判断实验中是向________________(填“酸”或“碱”,下同)溶液(待测液)中滴加________________溶液(标准液)。
(2)在这次测定中,为了指示中和反应刚好完全,用酚酞作指示剂,即在待测溶液中先滴入几滴酚酞试液,若看到________________, 则证明中和反应恰好完成。
(3)如果实验中使用的酸是硫酸,碱是氢氧化钠,且待测液和标准液的密度均以1.0g/mL计。若测定中取用待测液25mL,标准液溶质的质量分数为4.5%,根据图中数据,计算待测液溶质的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如右图是初中化学常用的部分实验仪器,据此回答问题:
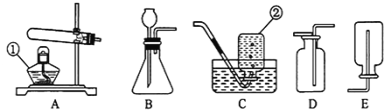
(1)写出标有序号的仪器名称:① , ② ;
(2)用氯酸钾制取氧气若用A装置,应该去掉 。
(3)应选用气体发生装置和收集装置为 (填字母编号)实验中,有同学发现对药品加热一段时间后收集不到氧气,可能的原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com