
| A. | 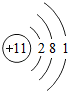 | B. | 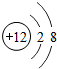 | C. | 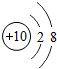 | D. | 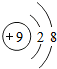 |
科目:初中化学 来源: 题型:选择题
| A. | 木炭在空气中充分燃烧:2C+O2$\frac{\underline{\;点燃\;}}{\;}$2CO;化合反应 | |
| B. | 甲烷燃烧:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+H2O;化合反应 | |
| C. | 加热高锰酸钾制取氧气:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$2K2MnO4+MnO2+O2↑;分解反应 | |
| D. | 加热铜丝:2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO;氧化反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 “低碳生活,绿色出行”.如图为潍坊公共自行车.请回答下列问题:
“低碳生活,绿色出行”.如图为潍坊公共自行车.请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 需要鉴别物质 | 方法1 | 方法2 |
| A | 厕所清洁剂与炉具清洁剂 | 加入鸡蛋壳 | 加入石蕊试液 |
| B | 硝酸钾和硫酸铵 | 加熟石灰研磨 | 加水溶解,再加入氯化钡溶液 |
| C | 氢氧化钠溶液和石灰水 | 通入二氧化碳 | 放置空气中是否潮解 |
| D | 羊毛和涤纶 | 点燃,闻气味 | 点燃,观察灰烬 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
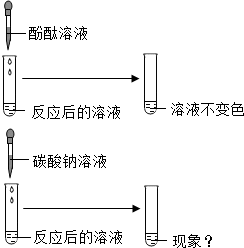 某实验小组的同学用氢氧化钠溶液和稀盐酸进行酸碱中和反应的实验时,向氢氧化钠溶液中滴加一定量的稀盐酸,发现忘记滴加指示剂了.此时,他们停止滴加稀盐酸,并对烧杯内所得溶液中的溶质成分进行探究.
某实验小组的同学用氢氧化钠溶液和稀盐酸进行酸碱中和反应的实验时,向氢氧化钠溶液中滴加一定量的稀盐酸,发现忘记滴加指示剂了.此时,他们停止滴加稀盐酸,并对烧杯内所得溶液中的溶质成分进行探究.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
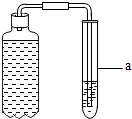 某同学用如图装置,利用碳酸饮料(如雪碧)中溶解的二氧化碳气体进行下列实验.请回答问题:
某同学用如图装置,利用碳酸饮料(如雪碧)中溶解的二氧化碳气体进行下列实验.请回答问题:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com