解:
(1)实验室制氢气常用常用锌与稀盐酸或稀硫酸反应制取,反应原理,Zn+H
2SO
4═ZnSO
4+H
2↑或者Zn+2HCl═ZnCl
2+H
2↑;
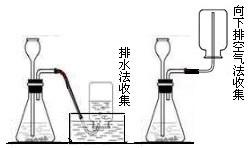
(2)实验室制氢气采用“固液 不加热”装置,且氢气难溶于水,密度比空气大,常用排水法或向下排空气法收集;
(3)根据酸的性质,金属活动性顺序表中排在氢前面的金属才能置换出酸中的氢,但排在镁之前的金属与酸反应太快,不
易收集,而锌活泼性适中,与酸反应能生成大量的氢气,所以实验室常用锌来制取氢气.
故答案为:(1)Zn+H
2SO
4═ZnSO
4+H
2↑或者Zn+2HCl═ZnCl
2+H
2↑;
(2)
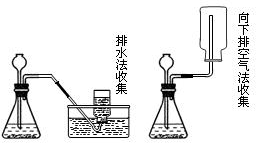
(3)活动性适中,易与盐酸或稀硫酸反应放出大量氢气.
分析:实验室制取氢气采用“固液 不加热”装置,常用锌与稀盐酸或稀硫酸反应来制取,金属必须是排在金属活动性顺序中(H)前面的金属,且活动性适中.
点评:要熟记实验室制取氢气的反应原理、实验步骤、装置示意图及其中仪器的名称、实验注意事项等,按照题目要求进行选择、填写或评价实验室制取氢气的实验步骤,或者画出、选配、评价装置示意图(或部分装置的示意图).

 :
:


 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案