
【题目】超细的铁微粒是一种纳米颗粒型材料,可在低温下将CO2分解为炭.下列推测不合理的( )
A. 超细铁微粒在反应中可能做催化剂
B. 该反应有助于减少温室气体排放
C. 该反应的另一产物可能是O2
D. 该反应属于化合反应
 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案科目:初中化学 来源: 题型:
【题目】为探究氢氧化钙溶液和稀盐酸反应所得溶液中溶质的成分,小鸣和同学们通过测定了反应后溶液的pH,得到了如下图所示的pH曲线,请回答:
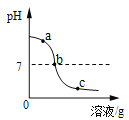
(1)由图可知该实验操作是将__________滴加到另一种溶液中;
(2)该反应的化学方程式为___________;
(3)实验过程中,小鸣取了a、b、c三处反应后的溶液于三个烧杯中,却忘了作标记,请你设计不同的方案(不再用测定pH的方法),探究三种样品分别属于哪处溶液。
【查阅资料】CaCl2溶液显中性,CaCl2+Na2CO3=CaCO3↓+2NaCl。
【探究过程】
①分别取少量样品于三支试管中,加入酚酞试液,观察到其中一支试管内出现___________的现象。结论:该样品是a处溶液。
②为进一步确定b或c处溶液,又设计了以下方案:
实验步骤 | 实验现象 | 实验结论 |
另取余下样品少量于两支试管中,分别滴加足量的Na2CO3溶液。 | ________ | 该样品为b处溶液。 |
【反思评价】探究反应后溶液中溶质的成分,除了要考虑生成物之外,还要考虑____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某兴趣小组用如图所示装置制取氧气,试管中固体的质量随时间变化的数据见下表。制取结束后,将剩余固体用适量水充分溶解后,过滤,回收二氧化锰固体,并得到氯化钾不饱和溶液100g。

加热时间/min | 0 | t1 | t2 | t3 |
固体质量/g | 28.0 | 23.2 | 18.4 | 18.4 |
(1)共制得氧气 g。
(2)计算所得氯化钾溶液的溶质质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铜片在潮湿的空气中久置,表面会产生绿色的铜锈。某小组同学设计并进行
实验,探究铜生锈的条件。
![]()
【猜想与假设】常温下,铜生锈可能与O2、CO2、水蒸气有关。
【进行实验】通过控制与铜片接触的物质,利用右图装置(铜片长
8cm,宽1cm,试管容积为20mL),分别进行下列7个实验,并持续观察30天。
编号 | 主要实验操作 | 实验现象 |
1 | 充满纯净的O2 | 铜片均无明显变化 |
2 | 充满纯净的CO2 | |
3 | 充满经煮沸并迅速冷却的蒸馏水 | |
4 | 加入蒸馏水5mL(液面未浸没铜片),再充满O2 | |
5 | 加入经煮沸并迅速冷却的蒸馏水5 mL,再充满CO2 | |
6 | 充入10mL O2,再充入10mLCO2 | |
7 | 加入蒸馏水5ml,再依次充入10mL CO2和10mL O2 | 铜片生锈,且水面附近锈蚀最严重 |
【解释与结论】
(1)实验3中,要使用经煮沸并迅速冷却的蒸馏水,原因是_______。
(2)实验5的目的是_______。
(3)通过上述实验,得出铜生锈的条件是_______。
【反思与评价】
(4)请写出一种防止铜制品锈蚀的方法_______。
(5)查阅资料可知,铜锈的主要成分是碱式碳酸铜,化学式为Cu2(OH)2CO3。由此,你认为上述实验中只需进行实验(填实验编号),就可探究出铜生锈条件,理由是_______。
(6)与以上进行的实验对比,你认为铜片在通常状况的空气中,生锈非常缓慢的原因
可能是_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】空气是一种宝贵的自然资源,下列气体不可直接从空气分离获得的是
A. 用作医疗急救的氧气 B. 用作焊接保护气的稀有气体
C. 用作食品防腐剂的氮气 D. 用作清洁燃料的氢气
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】区别二氧化碳、氧气和空气三种气体,应采用的方法是
A.将气体分别通入水中
B.将燃烧的木条分别伸入集气瓶中
C.将气体分别通入澄清的石灰水中
D.用带火星的木条分别伸入集气瓶中
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有30℃时的氯化钠饱和溶液,在下列情况下溶液中溶质的质量分数不变的是
A. 温度不变,向溶液中加入氯化钠晶体 B. 温度不变,向溶液中加入水
C. 升高温度蒸发掉一部分水,温度保持在40℃ D. 降温至10℃
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】同一个化学反应在不同条件下反应的快慢(即反应速率)是不同的。下列三组实验是探究不同条件对金属锌与盐酸反应速率的影响
实验操作 | 现象 | 结论 | |
第1组 |
| ①(选填“锌粒”或“锌粉”)反应更加剧烈。 | 反应物表面积越大,反应速率越大。 |
第2组 |
| 锌粒与20%的盐酸反应更加剧烈。 | 反应物② 越大,反应速率越大。 |
第3组 |
| 置于热水的试管反应更加剧烈。 | 温度越高,反应的速率越大。 |
(1)将表中的空格填写完整①_________②_________③__________
(2)请写出锌与稀盐酸反应的化学方程式_______________
(3)为了提高铁与盐酸反应的反应速率,请提出一种实验方案_____________
(4)综合其它实验结果,相同质量的铁、锌、铜与足量的稀盐酸反应产生氢气的质量关系如下图,其中正确的是__________(填选项)

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学实验室要从X、银、铜、锌四种金属混合物中分离某贵重金属.流程如下

其中错误的是
A.固体丙中一定只含银
B.四种金属活动性强弱顺序Zn、X、Cu、Ag
C.滤液C中只含有Cu(NO3)2
D.固体甲中一定含有Cu 和 Ag,可能含有X
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com