
分析 若向其中一份中加入足量的稀盐酸,充分反应后应得到0.4g不溶物,说明其中一份铁粉中含杂质0.4g;向另一份中加入足量的氯化铜溶液,充分反应得到不溶物2.0g,所得不溶物为铜与铁粉中杂质的混合物,则铜的质量=2.0g-0.4g=1.6g;根据生成铜的质量,由反应的化学方程式,可计算中其中一份铁粉中铁的质量,根据铁与硫酸反应的化学方程式,依据铁的质量即可计算硫酸的质量.
解答 解:(1)分析题意知原混合物的一半含杂质0.4克,则原混合物的一半生成铜的质量是2.0g-0.4g=1.6g;
(2)设原混合物与氯化铜反应的铁的质量为x
Fe+CuCl2═Cu+FeCl2
56 64
x 1.6g
$\frac{56}{x}=\frac{64}{1.6g}$
X=1.4g
设10g稀硫酸中溶质的质量为y
Fe+H2SO4═FeSO4+H2↑
56 98
1.4g y
$\frac{56}{1.4g}=\frac{98}{y}$
y=2.45g
所用稀硫酸的溶质质量分数:$\frac{2.45g}{10g}$×100%=24.5%;
答:(1)第二份样品充分反应后,得到铜的质量是1.6g
(2)第一份样品反应中所用稀硫酸的溶质质量分数是24.5%.
点评 解答本题需要使用杂质“迁移”,即两份相同的铁样品,其中所含杂质的质量一定也是相等的,这对本题的解决至关重要.


科目:初中化学 来源: 题型:多选题
| A. | 自来水经过加絮凝剂(明矾)、反应沉淀、过滤、活性炭吸附、投药消毒后提供给用户的过程中,只有投药消毒涉及到化学变化 | |
| B. | 硬水通过加热煮沸或蒸馏的方法可以得到软水,硬水加热过程中都涉及到化学变化 | |
| C. | 通过蒸馏可以得到最纯净的水.在蒸馏装置中,要插入一只温度计,测量沸水的温度,防止出现暴沸 | |
| D. | 过滤操作装置的要点是“一贴、二低、三靠”.如果过滤的速度慢是因为玻璃棒伸到了漏斗的底部,导致堵塞滤纸 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 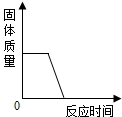 高温煅烧一定质量的石灰石 | |
| B. | 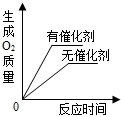 用等质量、等浓度的过氧化氢溶液分别制取氧气 | |
| C. | 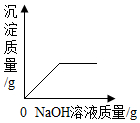 向一定质量的CuSO4溶液里滴加NaOH溶液 | |
| D. | 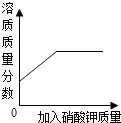 某温度下,向一定量饱和硝酸钾溶液中加入硝酸钾晶体 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
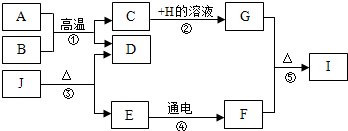 A~J分别为九年级化学学过的不同物质,它们存在如图所示的转化关系.已知A为铁锈的主要成分,E在常温下为液体,H的溶液呈蓝色,常温下B、D、F均为无色气体,其中J不稳定,受热易分解.(反应②、④的个别生成物已略去)
A~J分别为九年级化学学过的不同物质,它们存在如图所示的转化关系.已知A为铁锈的主要成分,E在常温下为液体,H的溶液呈蓝色,常温下B、D、F均为无色气体,其中J不稳定,受热易分解.(反应②、④的个别生成物已略去)查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 117g | B. | 46g | C. | 80g | D. | 106g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 第一次 | 第二次 | 第三次 | |
| O2质量(g) | 3 | 4 | 6 |
| SO2质量(g) | 6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com