

| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取样于试管中 | | 猜想②正确 相关的化学方程式 |
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取样于试管中 HCl(或Ca(OH)2溶液或CaCl2溶液) | 气泡冒出(或白色沉淀产生 | 猜想②正确;相关的化学反应方程式 Na2CO3+2HCl═2NaCl+H2O+CO2↑. (或Na2CO3+Ca(OH)2═CaCO3↓+2NaOH 或Na2CO3+CaCl2═CaCO3↓+2NaCl. |


科目:初中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题


查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
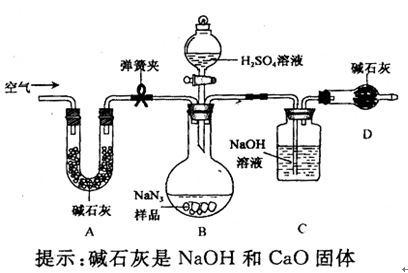
 (NaN3中的N全部转化为N2,其他产物略),反应中放出大量的热。
(NaN3中的N全部转化为N2,其他产物略),反应中放出大量的热。
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.小宇同学推测气体是氢气并检验 |
| B.小琪同学猜想CuCl2溶液呈酸性并测定 |
| C.小寒同学认为气体是氨气并检验 |
| D.小梁同学认为试剂变质,更换后再实验 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com