
分析 (1)复分解反应发生的条件:生成物要求必须含有沉淀,或者是气体,或者是水.
(2)根据图示直接回答问题;
(3)根据碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,结合反应的程度分析;
(4)根据碳酸钠和氢氧化钙不能共存分析;
(5)根据氢氧化钙能够和碳酸钠反应产生沉淀进行设计实验验证;
(6)①根据质量守恒定律分析;②根据化学方程式:Na2CO3+2HCl=2NaCl+H2O+CO2↑中CO2与Na2CO3的质量关系,可计算Na2CO3的质量,进一步计算样品中碳酸钠的质量分数.
解答 解:(1)复分解反应发生条件的是:生成物要求必须含有沉淀(难溶物),或者是气体,或者是水.
故选:C;
(2)根据图示知:用手在瓶口轻轻地扇动,让极少量气体飘进鼻孔(或不要把鼻孔凑到瓶口去闻气味);
(3)若碳酸钠过量,则含有碳酸钠、氢氧化钠;故填:NaOH、Na2CO3;
(4)碳酸钠和氢氧化钙不能共存,因此不可能同时存在;
(5)若猜想乙正确,则含有过量的氢氧化钙,因此可以滴加碳酸钠溶液,若产生白色沉淀,则含有氢氧化钙,
(6)①根据质量守恒定律,故反应中生成的气体质量:30g+100g-123.4g=6.6g;
②设碳酸钠质量为x
Na2CO3+2HCl=2NaCl+H2O+CO 2↑
106 44
x 6.6g
$\frac{106}{x}=\frac{44}{6.6g}$
x=15.9g
样品中碳酸钠的质量分数=$\frac{15.9g}{30g}$×100%=53%
答:样品中碳酸钠的质量分数为53%.
故答案为:(1)C;
(2)用手瓶口轻轻扇动使少量气体进入鼻孔;
(3)NaOH、Na2CO3;(4)不合理的是丙,因为Ca(OH)2和Na2CO3不能共存;
(5)滴加Na2CO3 溶液或通入CO2 现象:有白色沉淀生成.
(6)①6.6; ②53%.
点评 通过回答本题知道了在分析化学反应后所得物质的成分时,除了考虑生成物外,还需考虑反应物是否有剩余,两种物质发生反应时,若其中一种反应物有剩余,可判断另一种反应物一定完全反应.


 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:初中化学 来源: 题型:选择题
| A. | 属于一种新型的化合物 | B. | 可做散热材料 | ||
| C. | 可做新型电池的电极 | D. | 在一定条件下能与氧气反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 质子数相同的两种粒子一定属于同种元素 | |
| B. | 同种元素的原子结构和质量完全相同 | |
| C. | 元素的种类是由核内质子数决定的 | |
| D. | 元素是具有相同中子数的一类原子的总称 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 实验目的 | 实验操作 |
| A | 除去CO2中少量的CO | 点燃 |
| B | 除去CuSO 4溶液中的少量FeSO4 | 加入足量的铜粉 |
| C | 鉴别二氧化碳和氮气 | 用燃着的木条 |
| D | 鉴别硬水和软水 | 加入肥皂水 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 “可燃冰”(如图)主要成分是甲烷水合物,主要分布于深海沉淀物或陆域永久冻土中、1立方米的“可燃冰”可在常温下释放164立方米的甲烷和0.8立方米的淡水,被认为是一种潜力较大的能源之一.通常情况下,甲烷是没有颜色,没有气味的气体,比空气轻,极难溶于水.很容易燃烧
“可燃冰”(如图)主要成分是甲烷水合物,主要分布于深海沉淀物或陆域永久冻土中、1立方米的“可燃冰”可在常温下释放164立方米的甲烷和0.8立方米的淡水,被认为是一种潜力较大的能源之一.通常情况下,甲烷是没有颜色,没有气味的气体,比空气轻,极难溶于水.很容易燃烧查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 温度(℃) | 10 | 20 | 40 | 60 | 80 |
| KNO3 | 20.9 | 31.6 | 63.9 | 110 | 169 |
| NaCl | 35.8 | 36 | 36.6 | 37.3 | 38.4 |
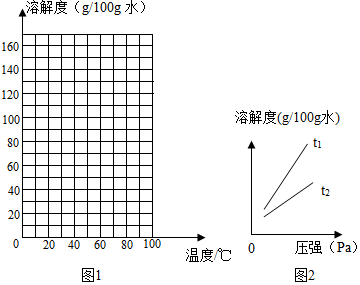
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
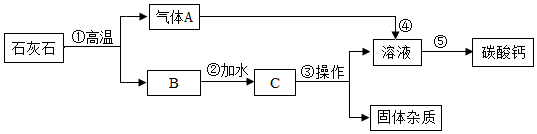
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com