
分析 (1)根据金属是否容易生锈考虑本题;
(2)根据金属材料的分类、炼铁的原理写出反应的方程式,根据防止铁生锈的措施分析回答.
解答 解:(1)金属活动性越强,越容易生锈,由“金龙纹手镯”光彩夺目,完好无损;铜镜表面有铜锈;铁器则锈迹斑斑,残存很少,可知铁最活泼,铜次之,金最不活泼.所以,三种金属的活动顺序由强到弱的顺序是 铁>铜>金;
(2)金属材料包括金属和合金,生铁和钢都是铁的合金,属于金属材料;炼铁的原理中反应物是一氧化碳和氧化铁,生成物是铁和二氧化碳,反应的方程式是:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,防止铁生锈的方法较多,例如:在铁制品表面镀一层其他金属,刷漆、涂油等.
故答为:(1)铁、铜、金;(2)金属材料,Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;刷漆、涂油等.
点评 解答本题关键是熟记金属活动性及其应用,熟练掌握方程式的书写方法.


科目:初中化学 来源: 题型:实验探究题
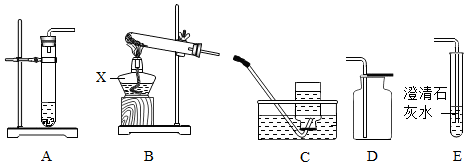
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
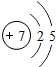 .
.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
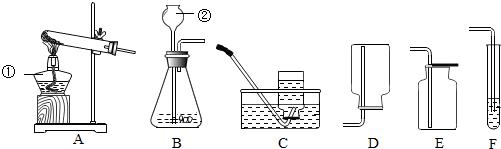
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com