
A.镁条在空气中燃烧后生成物的质量比原来镁条质量大
B.氯酸钾受热分解后,固体的质量比原来反应物的质量轻
C.蜡烛燃烧后,越来越短,最终消失
D.50mL酒精和50mL水混合后总体积一定是100mL
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案科目:初中化学 来源: 题型:阅读理解
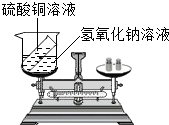 (2013?盐城二模)请你参与某学习小组的探究活动,并回答相关问题.
(2013?盐城二模)请你参与某学习小组的探究活动,并回答相关问题.| 实验方法及操作 | 可能观察到的现象 | 实验结论 |
取白色粉末少许置于试管中加稀盐酸 取白色粉末少许置于试管中加稀盐酸 |
有气泡产生 | 有碳酸钠存在 有碳酸钠存在 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com