
【题目】工业铁红主要成分是Fe2O3,还含有少量的FeO、Fe3O4。
[查阅资料]①草酸晶体(H2C2O4·3H2O)在浓硫酸作用下受热分解,化学方程式为:![]()
②碱石灰是固体NaOH和CaO的混合物,能吸收水蒸气和二氧化碳。
③铁的常见氧化物中铁的质量分数:
[问题讨论]为了测定铁红中铁的质量分数,小组间学生进行如下实验。
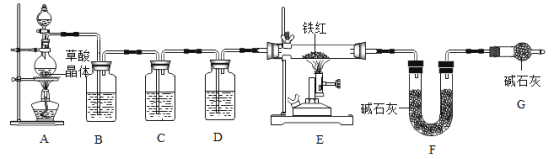
(1)实验前应先连接好仪器并_____。
(2)该实验为了保证进入E中的气体是纯净、干燥的CO,则B、C、D中的试剂依次是_____(填字母序号)。
a.浓硫酸
b.澄清的石灰水
c.氢氧化钠溶液
(3) C装置的作用是_____。
(4)写出E装置中所发生反应的一个化学方程式:_____。
(5)称取铁红样品1.0用上述装置进行实验,若实验价后称得F装置增重7.7g.则此铁红中铁元素的质量分数是_____。
[实验反思]
(1)如果缺少G装置(不考虑其他因素),则测得样品中铁的质量分数会_____(选填“偏小”“不变”“偏大”)。
(2)该实验装置的一个明显缺陷是_____。
【答案】检查装置的气密性 cba 证明CO2气体被吸收完全或检验CO2是否除净 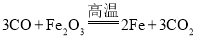 72.0% 偏小 缺少尾气处理装置
72.0% 偏小 缺少尾气处理装置
【解析】
问题讨论:
(1)有气体参与的反应需要检验装置气密性,所以实验前应先连接好仪器并检查装置气密性;
(2)进入E中的气体是纯净、干燥的CO,氢氧化钠能与二氧化碳反应,能吸收二氧化碳;二氧化碳能使澄清石灰水浑浊,澄清石灰水可检验二氧化碳是否除尽;浓硫酸具有吸水性,可干燥气体,干燥气体须放在最后一步,所以B、C、D中的试剂依次是氢氧化钠溶液、澄清石灰水、浓硫酸,故填:cba;
(3)氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,所以装置C的主要作用是证明CO2气体被吸收完全或检验CO2是否除净;
(4)E装置中所发生的反应是在高温条件下,氧化铁和一氧化碳反应生成铁和二氧化碳,化学方程式为: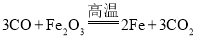 ;
;
(5)铁的氧化物与一氧化碳反应的化学方程式分别为:3CO+ Fe2O3![]() 2Fe + 3CO2,FeO+CO
2Fe + 3CO2,FeO+CO![]() Fe+CO2,Fe3O4+4CO
Fe+CO2,Fe3O4+4CO![]() 3Fe+4CO2,由反应的化学方程式可知,反应生成的二氧化碳中,氧元素一半来自于铁的氧化物,实验前后称得F装置增重7.7g就是二氧化碳的质量,因此铁红样品中氧元素质量为:
3Fe+4CO2,由反应的化学方程式可知,反应生成的二氧化碳中,氧元素一半来自于铁的氧化物,实验前后称得F装置增重7.7g就是二氧化碳的质量,因此铁红样品中氧元素质量为:![]() ,所以铁红中铁元素的质量分数=
,所以铁红中铁元素的质量分数=![]() ;
;
实验反思:
(1)碱石灰可以吸收空气中的二氧化碳和水,如果缺少G装置,F中吸收的二氧化碳质量增多,计算出的氧元素的质量增多,所以测得样品中铁的质量分数会偏小;
(2)一氧化碳有毒,扩散到空气中污染环境,所以本实验装置的一个明显缺陷是缺少尾气处理装置。


 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案科目:初中化学 来源: 题型:
【题目】甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( )
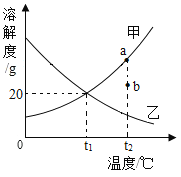
A. t1℃时,甲、乙两种溶液中溶质的质量相等
B. t1℃时,100g甲物质的饱和溶液中溶质的质量是20g
C. 要将甲溶液的状态由a点转化为b点,可以加适量溶剂
D. 分别将t2℃时两种物质的饱和溶液降温至t1℃,均有晶体析出
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验一:根据如图所示实验装置回答问题:

(1)写出B中两种仪器的名称(导管利胶塞除外)_。
(2)实验室用高锰酸钾制取较纯净的氧气,选择的发生装置和收集装置是__(填字母),反应的化学方程式是____。
(3)实验室用锌粒和稀硫酸反应制取氢气,若用G装置收集氢气,气体应从__(填“a ”或“b”)处通入。
实验二:实验室制取二氧化碳是中学化学的一个重要实验,同学们在制出二氧化碳后又进行了相关的系列实验,实验装置如图:
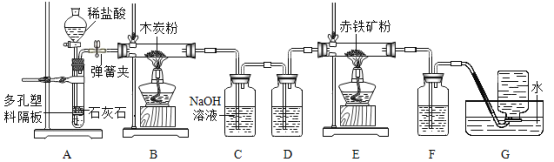
(1)用A装置制气体的最大优点是可以___。B裝置的现象:____。
(2)D装置可以吸收气体中的水蒸气,D装置中盛放的药品是_____。
(3)E装置中发生反应的实验现象为___,F装置中盛放的药品是__。
(4)G装置的作用是___。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2019年3月10日,我国自主研制的代表世界最先进水平的载人深潜器“深海勇士”号,在西南印度洋圆满完成下潜到4500米深度进行科考的预定任务。请回答下问题:
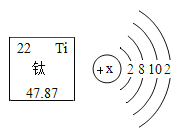
(1)潜水器的外壳材料主要是钛合金和特种钢,已知钛在周期表中的信息及钛原子的结构示意图如图所示:图中x=_____;钛的相对原子质量为_____。
(2)“深海勇士”带回来的资料和照片表明海底有甲烷渗漏现象,此现象与可燃冰有关。甲烷是三大化石燃料中_____的主要成分。
(3)海底有大量的多金属结核,多金属结核的加工方法之一为硫酸浸出法:在一定条件下用硫酸溶解,使铜转化为硫酸铜,再通入硫化氢(H2S)使硫酸铜转化为硫化铜(CuS)沉淀,硫化铜经焙烧转化为氧化铜。请用化学方程式表示将硫酸铜转化为硫化铜:_____,硫化铜焙烧时发生的反应为 ,则X的化学式为_____。
,则X的化学式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在如图所示的转盘中,序号①—④分别代表碳酸钠、硫酸、硫酸铜、氢氧化钙四种物质中的一种,其中③和④是配制农药波尔多液的成分,且图中相邻的物质(或其溶液)在常温下能相互发生化学反应。
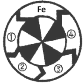
(1)硫酸应位于转盘上__________(填序号)处的位置。图中④代表的物质是一种_______(填“酸”“碱”或“盐”)。
(2)②与③反应的化学方程式为___________________________________。
(3)①与③___________(填“能够”或“不能”)发生化学反应。
(4)下列物质能替代转盘上“铁”的位置的是________(填标号)。
A 汞 B 镁 C 氢氧化钠 D 氯化钠
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】同学们,再过十几天你们即将离校,那一天请你们再看看书,我再看看你们!

(1)俗语说:“冬至饺子夏至面”,一般东北人比较爱吃的面有打卤面和炸酱面等。打卤面中主要营养成分在人体中最终转化为能被人体直按吸收的营养素的化学式为_________,卤一般为茄子肉丁或尖椒肉丝,这两种卤中富含的较多的不能提供能量的营养素是(除水外)______,除此之外卤子中往往比普通菜中加入的食盐更多,食盐中富含的主要营养素有些能够_________,促进身体健康,有的还是构成人体组织的重要材料。
(2)鸡蛋富含蛋白质,蛋白质是由多种氨基酸构成的极为复杂的______(填物质分类),人体获得的蛋白质,在体内先转化成氨基酸,部分氨基酸被氧化生成尿素、水和二氧化碳,由此可知蛋白质是由______(填写元素符号)元素组成的。
(3)东北方种植蔬菜过程中。为增强作物抗寒抗旱能力并使蔬菜叶生长茂盛,叶色浓绿。选择施加的一种化肥是__________(填写名称)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人类的生产、生活离不开水和溶液。
(1)自来水厂净水过程中使用了活性炭,这是因为活性炭具有_________作用。
(2)现有软水和硬水样品各一瓶,请设计实验对它们进行区分,并完成实验报告。
实验步骤 | 实验现象及结论 |
____ | ____ |
(3)下表是氯化钠、硝酸钾在不同温度时的溶解度。
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | |
溶解度/g | 氯化钠 | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 | 38.4 |
硝酸钾 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 | |
下列说法正确的是_________(填字母)。
A 氯化钠的溶解度大于硝酸钾的溶解度
B 20℃时,将30g氯化钠加入50 g水中,充分搅拌,所得溶液中溶质的质量分数为37.5%
C 分别将80℃时硝酸钾的饱和溶液和氯化钠的饱和溶液降温至30℃,析出硝酸钾晶体的质量比析出氯化钠晶体的质量大
D 从含有少量氯化钠的硝酸钾的饱和溶液中得到较多的硝酸钾晶体,通常可采用冷却热饱和溶液的方法
(4)下图是一定溶质质量分数的氯化钠溶液的配制流程。
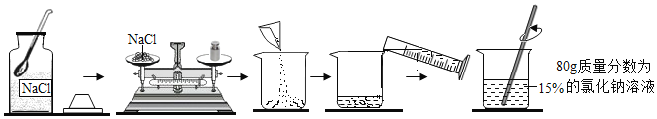
①实验步骤依次为:_________、称量、量取、溶解。用量筒量取所需的水时,若采用仰视的方法读数,配制的氯化钠溶液中溶质的质量分数会_________(填“偏大”或“偏小”)。
②将20g质量分数为6%的氯化钠溶液与30g质量分数为4%的氯化钠溶液充分混合,所得溶液中溶质的质量分数为_________。
(5)在0℃时,氮气的溶解度为0.024。这句话的含义是_______________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以甲为原料合成化工产品丁的微观过程如图所示,下列说法正确的是( )
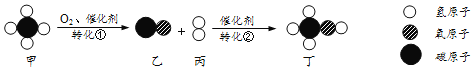
A. 乙、丁为氧化物
B. 转化①中乙和丙的分子个数之比为1∶1
C. 该反应前后原子总数发生了改变
D. 该过程体现了无机物与有机物可相互转化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com