
| A. | H2SO4 | B. | 石灰石的主要成分 | ||
| C. | 氯酸钾 | D. | 蒸馏水 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 如图是测定空气中氧气含量的实验装置.下列有关该实验的说法正确的是( )
如图是测定空气中氧气含量的实验装置.下列有关该实验的说法正确的是( )| A. | 使用红磷的量越多,最终进入集气瓶的水也越多 | |
| B. | 若实验过程中没有夹紧止水夹或燃烧匙插入集气瓶的速度太慢,都会影响测定的结果 | |
| C. | 本实验可以证明空气含有N2、O2、CO2和稀有气体 | |
| D. | 燃烧匙中的红磷可以换成硫或木炭 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
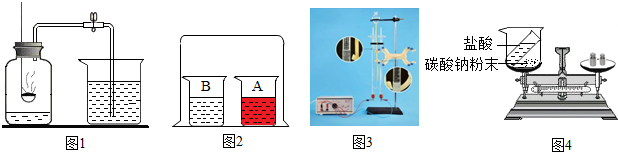
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 澄清石灰水和烧碱溶液(稀盐酸) | |
| B. | 硫酸铜溶液和高锰酸钾溶液(观察颜色) | |
| C. | 乙醇和食盐水(闻气味) | |
| D. | 纯碱溶液和稀硫酸(酚酞试液) |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
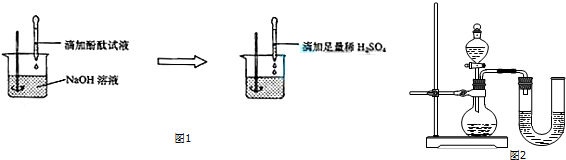
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com