

分析 (1)根据仪器名称分析;
(2)根据气体的密度分析;
(3)根据气体的性质结合装置特点进行分析;
(4)根据二氧化碳与氢氧化钠溶液反应生成碳酸钠和水分析.
(5)①根据实验室常用吸收二氧化碳,干燥气体的试剂进行分析解答.
②根据A装置中的试剂和AB装置的反应原理进行分析解答.
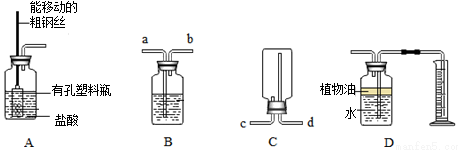
解答 解:(1)仪器X是广口瓶,故填:广口瓶;
(2)用如图1装置收集气体时,若从a处进气,则收集的气体密度比空气大;若从b处进气,则收集的气体密度比空气小,可以是氢气,故填:大;H2;
(3)在仪器X中加入满瓶的水,可用于排水法收集气体,因为气体的密度比水小,此时气体应从 a进气,若进气的方向相反,则出现的现象是气体从b逸出,收集不到,故填:a;气体从b逸出,收集不到;
(4)在仪器X中加入某种溶液(如图3),可以用于除去混合气体中的某种成分,如除去CO中的CO2气体,可以在X中加入烧碱溶液,二氧化碳与氢氧化钠溶液反应的化学反应方程式是CO2+2NaOH═Na2CO3+H2O,故填:CO2+2NaOH═Na2CO3+H2O.
(5)①依据实验要求可知A、B装置应分别为除杂和干燥装置,根据一氧化碳和二氧化碳的性质可知A是用以吸收CO2的,因此AB应分别装NaOH溶液和浓H2SO4,A吸收CO2后生成碳酸钠,最后还应将其释放出来,从题目给出的试剂看,显然分液漏斗中盛放的是稀硫酸,与碳酸钠反应生成二氧化碳,故填:浓硫酸;稀硫酸;
②广口瓶中盛放的是氢氧化钠,会吸收二氧化碳,而一氧化碳不会与氢氧化钠反应,将一氧化碳分离,发生反应的化学方程式为CO2+2NaOH=Na2CO3+H2O;待该气体收集完毕时,接下来的实验操作是关c开d.
故答案为:CO;关c开d; CO2+2NaOH=Na2CO3+H2O.
点评 利用化学的方法对一氧化碳和二氧化碳的分离,要根据气体的性质选取净化剂,气体净化的原则是:不减少被净化气体的量,不引进新的杂质,操作简便,易于分离.


科目:初中化学 来源: 题型:选择题
| A. | 与酸反应产生二氧化碳气体的盐一定含有碳酸根 | |
| B. | 达稳定结构的原子最外层电子数一定为8 | |
| C. | 物质与氧气的反应一定属于氧化反应 | |
| D. | 碱中一定含有金属元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 4个 | B. | 5个 | C. | 6个 | D. | 7个 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | 甲的化学式为H2O | |
| B. | 反应中甲、乙、丙、丁的分子个数比为1:1:1:1 | |
| C. | 若32g乙参加反应,则生成18g丁 | |
| D. | 丁中氧元素的质量一定等于参加反应的乙的质量 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com