
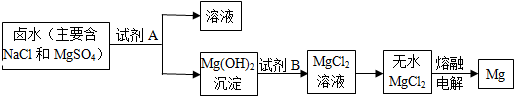
���� ��1�����ݺ�ˮ�ijɷּ���ô��εķ�����������
��2�����ݻ����Һ���ᴿ����������
��3����������þת��Ϊ������þ������Ҫ�������Һ��������þ����������ˮ�������ᷴӦ���з������
��4�����ݷ�Ӧ��������Ӧ�����������غ㶨��д����ѧ��Ӧʽ��
��� �⣺��1����ˮ�к������Ļ�ѧ������ˮ��������Ȼ��ƣ��Ӻ�ˮ����ȡ����õķ�����������
�ʴ�Ϊ���Ȼ��ƣ� ����
��2����������ˮ�����˺�õ�����Һ�к���MgSO4��CaCl2��NaCl����������Һ�м���������NaOH��Һ����ʱ�õ��Ļ����Ϊ��
Mg��OH��2������Na2SO4��Ca��OH��2������NaOH��NaCl������յõ��Ļ���м��������BaCl2��Һ����ʱ�õ��Ļ����Ϊ��Mg��OH��2������BaSO4������Ca��OH��2������NaOH��NaCl��BaCl2�����������м��������Na2CO3��Һ���õ��Ļ����Ϊ��Mg��OH��2������BaSO4������CaCO3������NaOH��BaCO3������NaCl��Na2CO3���˻���ᆳ���˺�õ�NaOH��NaCl�Ļ����Һ����ʱ�������������ᣬ���ɵõ��ϴ������Ȼ�����Һ��
��3������þת��Ϊ������þ������Ҫ�������Һ�������зḻ��ʯ��ʯ��Դ������ʯ��ʯ���Եõ������ƣ�������������ˮ���Ƶ�����������Һ������A�Լ�Ӧ������������Һ��
������þ����������ˮ�������ᷴӦ����������þ����ת��Ϊ�Ȼ�þ����ѡ��������þ��ϡ���ᷴӦ�������Ȼ�þ��ˮ������B�Լ�Ӧ��ϡ������Һ��
��4���ٷ�Ӧ�����Ȼ�����Һ��������������̼��������������̼�����ƾ��壬�÷�Ӧ�Ļ�ѧ����ʽΪ��NaCl+NH3+H20+C02=NaHCO3+NH4Cl��
�ڸ��ݼ���̼�����ƾ�����Ƶô����֪��Ӧ����̼�����ƣ���Ӧ�����Ǽ��ȣ����������д���÷�Ӧ�Ļ�ѧ����ʽΪ��2NaHCO3$\frac{\underline{\;\;��\;\;}}{\;}$Na2CO3+CO2��+H2O��
�ʴ�Ϊ����1��NaCl����������2���ڢ٢ܢۣ���3���������ƣ�ϡ�����4����NaCl+NH3+H20+C02=NaHCO3+NH4Cl����2NaHCO3$\frac{\underline{\;\;��\;\;}}{\;}$Na2CO3+CO2��+H2O��
���� Ҫ�����������Ŀ�����ȣ�Ҫ�������ǶԺ�����Դ�ĺ������������ã��Լ���֮��ص�֪ʶ��Ȼ���������������龰�����ѧ�����֪ʶ�ͼ��ܣ���ϸ�ĵ�̽��������������ĿҪ����������ѡ����ɣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���Ӻ�ԭ�Ӷ��ڲ����˶����������Ǿ�ֹ�� | |
| B�� | ���ʯ����ԭ�ӹ��ɵģ�����þ�������ӹ��ɵ� | |
| C�� | ͬһԪ�ص��������ӣ���ԭ�Ӻ���������һ����ͬ | |
| D�� | ��ԭ��ʧȥ���ߵõ����Ӻ������ʷ����˸ı� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| NH3 | N2 | NO | NO2 | |
| �ɫ | ��ɫ | ��ɫ | ��ɫ | ����ɫ |
| �ܽ��� | ��������ˮ | ������ˮ | ������ˮ | ������ˮ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������


 ���ܽ�����ش��������⣺
���ܽ�����ش��������⣺| �¶�/�� | 10 | 30 | 50 | 60 | |
| �ܽ��/g | NaCl | 35.8 | 36.3 | 37.0 | 37.3 |
| KNO3 | 20.9 | 45.8 | 85.5 | 110 | |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
| ʵ�鲽�� | ʵ������ | ʵ����� |
| ��ȡ�����Թ��е��ϲ���Һ���μ�1��2�η�̪��ҹ | ��Һ�ʺ�ɫ | ��ɫ��ĩ������������ |
| ���������Թܲ����İ�ɫ�����м������ϡ���� | �����ݲ��� | ��ɫ��ĩ�к���CaCO3 |
| ʵ�鷽�� | ����ҺpH | �μ�Na2CO3��Һ | �μ�BaCl2��Һ |
| ʵ����� |  | 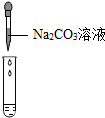 | 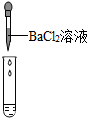 |
| ʵ������ | ��ֽ��ɫ�����ձ�ɫ����pH��7 | �����ݲ��� | ������ɫ���� |
| ʵ����� | ��Һ����H2SO4 | ��Һ����H2SO4 | ��Һ����H2SO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ˮ�����Ƶô���ˮ | |
| B�� | �õ����ϳɰ� | |
| C�� | �ô����Ƶ��ռ� | |
| D�� | ��һ�������£���ʯīת��Ϊ���ʯ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �綯���г��㷺ʹ�ô������ϣ���ͼ��ʾ��
�綯���г��㷺ʹ�ô������ϣ���ͼ��ʾ���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com