
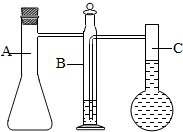
 某同学利用图所示实验装置来测定镁元素的相对原子质量.
某同学利用图所示实验装置来测定镁元素的相对原子质量.分析 镁和稀硫酸反应生成硫酸镁和氢气;
根据提供的数据可以计算镁的相对原子质量.
解答 解:(1)这里C装置的作用是测量氢气的体积.
故填:测量氢气的体积.
(2)设镁的相对原子质量为x,
反应生成氢气的质量为:0.09g/L×(600mL-400mL)×10-3=0.018g,
Mg+H2SO4═MgSO4+H2↑,
x 2
0.2g 0.018g
$\frac{x}{0.2g}$=$\frac{2}{0.018g}$,
x=22.2,
①如果镁片中含有与硫酸不反应的杂质,会导致生成氢气的质量偏小,从而导致计算出的相对原子质量偏大;
②如果没有除去镁片表面的氧化膜,会导致生成氢气的质量偏小,从而导致计算出的相对原子质量偏大;
③如果镁片中含有杂质铝,会导致生成氢气的质量偏大,从而导致计算出的相对原子质量偏小.
故填:22.2;③.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验编号 | 实验操作 | 实验现象 |
| ① | 加入适量稀硫酸 | 有微量气泡,固体全部溶解,得到无色澄清溶液 |
| ② | 加入适量蒸馏水 | 固体部分溶解 |
| ③ | 加入适量无水乙醇 | 固体部分溶解 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
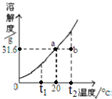 甲是初中化学中的常见物质,请根据下列叙述回答问题.
甲是初中化学中的常见物质,请根据下列叙述回答问题.| 实验操作 | 实验结果 |
| 取20mL水,加入5g KNO3,搅拌,恢复至20℃ | 全部溶解,得溶液① |
| 再加X g KNO3,搅拌 | 恰好饱和,得溶液② |
| 再加5g KNO3,搅拌 | 得溶液 ③ |
| 加热 | 全部溶解,得溶液④ |
| 冷却至20℃ | 晶体析出,母液⑤ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
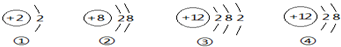
| A. | ①②④均属于稀有气体元素的原子 | B. | ①③均易失去2个电子 | ||
| C. | 1个②粒子带2个单位的负电荷 | D. | ③④属于同种粒 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com