
【题目】请结合如图回答问题:
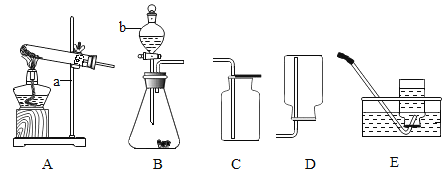
(1)写出图中有标号仪器的名称:a___________,b_________________。
(2)用高锰酸钾制取一瓶氧气,可选用装置A和__________(选填序号)组合。装入药品前要先_________,该反应的化学方程式为_________________________。
(3)用双氧水和二氧化锰制氧气,二氧化锰的作用是__________,可选用的发生装置是_________(选填序号)。
科目:初中化学 来源: 题型:
【题目】水是生命之源,请回答下列问题:
(1)水由 组成,由 构成.
(2)饮用水的质量关系人的健康.生活中常采用 的方法降低饮用水的硬度.
除去饮用水的异味可采用的物质是 ,测定饮用水的酸碱度,可使用 .高铁酸钾(K2FeO4)是一种“绿色”环保高效净水剂,可由如下反应制得:Fe2O3+3X+4KOH![]() 2K2FeO4+3KNO2+2H2O,则X的化学式为 ,K2FeO4中Fe的化合价为 .
2K2FeO4+3KNO2+2H2O,则X的化学式为 ,K2FeO4中Fe的化合价为 .
(3)水是常用的溶剂,将下列物质分别加入水中,充分搅拌后,不能形成溶液的是
A.白糖 B.白醋 C.白酒 D.麻油.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有A、B、C三种元素,A是地壳中含量最丰富的元素,B的单质在A的单质中燃烧时发出明亮的蓝紫色火焰,生成有刺激性气味的气体D,C原子的原子核外有12个电子。请回答下列问题:
(1)A的元素符号为________,C元素的名称为________。
(2)D的化学式为______。
(3)B单质在A单质中反应的文字表达式为____,该反应的基本反应类型为___反应。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】O2的来源。
(1)实验室制取O2。
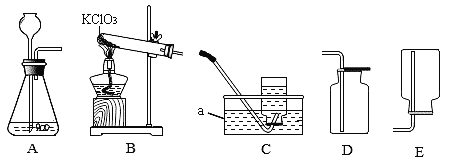
①仪器 a 的名称是_______。
②实验室用KClO3制取O2的化学方程式是___;用酒精灯给试管内固体加热应注意先_____,然后对固体所在部位加热;收集O2可选用的装置是___(填序号)。
③用过氧化氢溶液制取O2时,为避免剧烈反应,可从仪器、试剂、操作等方面进行控制, 结合装置 A 写出一条合理措施_______;反应后剩余药品不要随意丢弃,应________。
(2)自然界生产O2。
①图 1 为自然界中O2的主要来源,其中海洋藻类的光合作用是供氧主力,请将化学方程式补充完整:xCO2+ _______  (CH2O)x+xO2+xH2O。
(CH2O)x+xO2+xH2O。
②图 2 用N2从海水中吹出CO2并用碱液吸收,进一步实验测量海水中无机碳的含量。画出虚线框中的缺损的部分________,最右侧 NaOH 溶液的作用是_______。
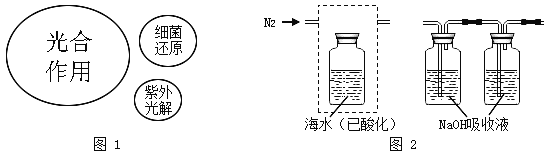
③为保护环境,实验后的海水调节 pH 后重新排回大海,以下说法正确的是______。
A 调节成与排放区域海水相同的 pH
B 调节成弱酸性防止溶解更多的二氧化碳
C 调节成弱碱性吸收更多的二氧化碳,缓解温室效应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图像中有关量的变化趋势与对应叙述关系正确的是
A.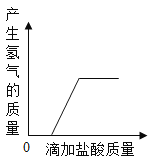 向一定质量表面生锈的铁片中滴加盐酸至过量
向一定质量表面生锈的铁片中滴加盐酸至过量
B.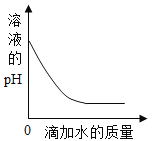 向一定质量的稀硫酸中滴加水
向一定质量的稀硫酸中滴加水
C.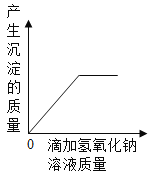 向盐酸和氯化铁的混合溶液中滴加氢氧化钠溶液至过量
向盐酸和氯化铁的混合溶液中滴加氢氧化钠溶液至过量
D.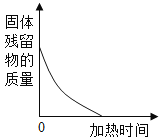 高温煅烧一定质量的石灰石
高温煅烧一定质量的石灰石
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列实验不能到成实验目的的是
A | B | C | D | |
目的 | 检验装置气密性 | 测定空气中 氧气的含量 | 控制反应的 开始与停止 | 证明氢氧化钠与二氧化碳反应 |
实验 |
|
|
|
|
A.AB.BC.CD.D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铟元素相关信息如图所示,下列说法正确的是( )
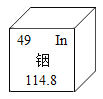
A.铟元素属于非金属元素
B.铟原子的中子数为49
C.铟原子的核外电子数为114
D.铟原子的相对原子质量为114.8
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室常用MnO2与浓盐酸反应制备C12,反应的化学方程式为![]() ,反应装置如图1所示。
,反应装置如图1所示。
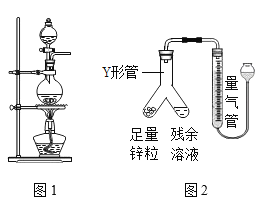
(1)检查装置气密性之后的操作依次是_________(填字母)。
A向烧瓶中加入MnO2粉末
B加热
C向烧瓶中加入浓盐酸
(2)制备反应会因盐酸浓度下降而停止。为测定反应残余溶液中盐酸的浓度,探究小组同学提出下列实验方案:
①甲同学的方案:利用盐酸和硝酸银反应,化学方程式为______________,利用残余溶液与足量的AgNO3溶液反应,称量生成沉淀的质量,可以测出反应残余溶液中盐酸的浓度。此方案是否可行,请说明原因:______________________。
②乙同学的方案:与足量Zn反应,测量生成的气体体积。实验装置如图2所示(夹持装置已略去)。使Y形管中的残余溶液与锌粒反应的正确操作是将_____________转移到_________________中。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】CaCO3广泛存在于自然界,是一种重要的化工原料。某种大理石除主要成分CaCO3外,还含有少量的硫化钙。小李和小明同学用这种大理石和盐酸反应,分别开展以下探究,请你参与探究并回答相关问题。
[查阅资料]
资料一:已知复分解反应![]() 可自发进行。在常温下,测得浓度为a%的下列五种溶液的pH大小情况如下表所示:
可自发进行。在常温下,测得浓度为a%的下列五种溶液的pH大小情况如下表所示:
溶质 | H2SO4 | HCl | H2S | H2CO3 | HClO |
pH | 小→大 | ||||
表中pH大小情况揭示出复分解反应的一条规律,即较强酸发生类似反应可以生成较弱酸。下列反应均能发生,其中不符合该规律的是_____________(填字母代号)。
A![]()
B![]()
C![]()
D![]()
资料二:常见的干燥剂有①浓硫酸、②无水氯化钙、③氢氧化钠固体、④生石灰、⑤五氧化二磷。
[实验探究]小茜同学为了得到纯净的二氧化碳,设计了如图所示装置,请你分析:
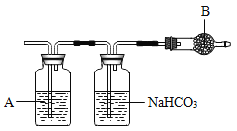
(1)制备的二氧化碳气体中,可能含有的杂质是____________。
(2)上述装置中,A是______________溶液,NaHCO3溶液可以吸收_____________。
(3)上述装置中,B物质不可能是_________(填字每代号)。
A五氧化二磷 B无水氯化钙 C氢氧化钠固体 D生石灰
(4)如果B失效,则得到的二氧化碳质量__________(“偏高”“偏低”或“不受影响”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com