
| 溶液 | 外观 | pH | 溶液成分 | |
| 甲 | 无色、透明 | >7 | ? | ? |
| 乙 | 无色、透明 | =7 | Ba(NO3)2 | ? |
| 丙 | 无色、透明 | <7 | ? | ? |
分析 (1)①根据草木灰显碱性,铵态氮肥和碱混合会生成氨气进行分析;
②根据气体的溶解度随温度的升高而减小进行分析;
③根据农药在使用时应该合理使用进行分析;
④根据撒盐可以降低水的凝固点进行分析;
(2)根据硫酸钡难溶于水,碳酸钡和盐酸反应会生成氯化钡、水和二氧化碳,要想解毒,应将可溶性钡盐转化为不溶性性钡盐进行分析;
(3)根据氢氧化钠具有强烈的腐蚀性,碳酸氢钠和盐酸反应会生成二氧化碳进行分析;
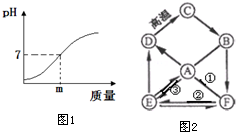
(4)根据熟石灰与盐酸反应生成氯化钙与水,依据图象中pH值的变化是从小于7逐渐的增大到大于7,当加入溶液的质量为mg时,溶液的pH小于7进行分析;
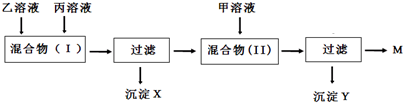
(5)根据A、B、C、D、E、F均为初中化学常见的物质,D在生活中常用作补钙剂和建筑材料,所以D是碳酸钙,F为NaOH,E和氢氧化钠可以相互转化,E会转化成碳酸钙,所以E是碳酸钠,碳酸钠和A可以相互转化,A会与氢氧化钠反应,所以A是二氧化碳,碳酸钙高温会生成C,所以C是氧化钙,氧化钙会生成B,B会与二氧化碳反应,所以B是氢氧化钙,然后将推出的物质进行验证即可;
(6)①根据污水分析情况和溶液的PH来分析一定有的物质,并根据离子的共存来判断可能有的物质;
②根据其可能的成分来书写对应的化学反应方程式;
③将六种物质中的离子混合后,利用只有K+和NO3-存在,其余离子转化为沉淀或水来解答.
解答 解:(1)①草木灰显碱性,铵态氮肥和碱混合会生成氨气,故①错误;
②气体的溶解度随温度的升高而减小,故②正确;
③农药在使用时应该合理使用,故③错误;
④撒盐可以降低水的凝固点,故④正确;
故选:②④;
(2)透视时通常服用一种乳白色的液体“钡餐”,其主要成分是BaSO4,该液体属于悬浊液,已知含Ba2+的溶液会使人中毒,若误服BaCO3会中毒,这是由于碳酸钡和盐酸反应会生成氯化钡、水和二氧化碳,化学方程式为:BaCO3+2HCl=BaCl2+H2O+CO2↑,若误服,应立即服泻盐MgSO4,MgSO4能与氯化钡反应生成既不溶于水也不溶于酸的硫酸钡沉淀,化学方程式为:BaCl2+MgSO4=BaSO4↓+MgCl2;
(3)氢氧化钠具有强烈的腐蚀性,碳酸氢钠和盐酸反应会生成二氧化碳,会加剧胃溃疡的病情,所以应服用含有Al(OH)3的药物,氢氧化铝和盐酸反应会生成氯化铝和水,化学方程式为:Al(OH)3+3HCl=AlCl3+3H2O;
(4)氢氧化钙和盐酸反应能生成氯化钙和水,化学方程式为:Ca(OH)2+2HCl=CaCl2+2H2O;
当加入熟石灰mg时,溶液的pH小于7,溶液显酸性,盐酸有剩余,所得溶液的pH<7;
(5)①A、B、C、D、E、F均为初中化学常见的物质,D在生活中常用作补钙剂和建筑材料,所以D是碳酸钙,F为NaOH,E和氢氧化钠可以相互转化,E会转化成碳酸钙,所以E是碳酸钠,碳酸钠和A可以相互转化,A会与氢氧化钠反应,所以A是二氧化碳,碳酸钙高温会生成C,所以C是氧化钙,氧化钙会生成B,B会与二氧化碳反应,所以B是氢氧化钙,经过验证,推导正确,所以E是Na2CO3;
②C→B的反应是氧化钙和水反应生成氢氧化钙,化学方程式是:CaO+H2O=Ca(OH)2;
③碳酸钙高温分解属于分解反应,氧化钙和水反应生成氢氧化钙属于化合反应,碳酸钠和氢氧化钙反应生成碳酸钙和氢氧化钠属于复分解反应,所以没有涉及的化学基本反应类型是:置换反应;
(6)①因甲的PH>7,上述六种物质只有KOH为碱,则一定有KOH;已知溶液中不可能同时存在Ag+和OH-,则甲中不会有AgNO3,又乙中一定有Ba(NO3)2,丙中的PH<7,则丙中一定含有HNO3,根据物质的共存可知甲中可能有K2SO4或KCl,则乙和丙混合时得到X沉淀的成分有两种情况,①若甲中有KOH和K2SO4,则乙和丙混合生成AgCl沉淀;②若甲中有KOH和KCl,则乙和丙混合生成BaSO4沉淀;
②若甲中有KOH和K2SO4,则乙和丙混合生成AgCl沉淀后的滤液中主要有Ba(NO3)2和HNO3,则发生的反应为:
K2SO4+Ba(NO3)2═BaSO4↓+2KNO3;HNO3+KOH═H2O+KNO3;
若甲中有KOH和KCl,则乙和丙混合生成硫酸钡沉淀后滤液中主要有HNO3和AgNO3,则发生的反应为:
KCl+AgNO3═AgCl↓+KNO3;HNO3+KOH═H2O+KNO3;
③因六种物质两次混合均完全反应,混合时生成硫酸钡和氯化银沉淀及水,而钾盐和硝酸盐都能溶于水,则两次混合后M溶液中的溶质为KNO3,其中的K、N是植物生长的营养元素.
故答案为:(1)②④;
(2)悬浊液,BaCO3+2HCl=BaCl2+H2O+CO2↑,BaCl2+MgSO4=BaSO4↓+MgCl2;
(3)Al(OH)3,Al(OH)3+3HCl=AlCl3+3H2O;
(4)Ca(OH)2+2HCl=CaCl2+2H2O,<;
(5)①Na2CO3;
②CaO+H2O=Ca(OH)2;
③置换反应;
(6)①KOH,K2SO4(或KCl),AgCl(或BaSO4);
②K2SO4+Ba(NO3)2═BaSO4↓+2KNO3;HNO3+KOH═H2O+KNO3或KCl+AgNO3═AgCl↓+KNO3;HNO3+KOH═H2O+KNO3;
③KNO3,K、N.
点评 本题较难,考查利用信息及复分解反应发生的条件来处理工厂污水问题,学生应学会结合所学知识并灵活应用知识来解决实际问题,还要注意考虑问题要全面,比如本题三个厂污水中可能含的物质有几种可能性,针对不同情况发生的反应是不同的.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | CuO+H2SO4═CuSO4+H2O | B. | Na2CO3+2HCl═2NaCl+CO2↑+H2O | ||
| C. | Cu(OH)2+2HCl═CuCl2+2H2O | D. | Ca(OH)2+CO2═CaCO3↓+H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
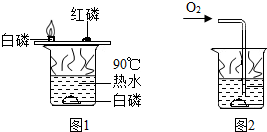 小明用图1所示装置探究可燃物燃烧的条件.他发现热水中的白磷熔化成一白色小液滴.不久,铜片的白磷开始燃烧,而红磷和水中的白磷都不燃烧.请回答:
小明用图1所示装置探究可燃物燃烧的条件.他发现热水中的白磷熔化成一白色小液滴.不久,铜片的白磷开始燃烧,而红磷和水中的白磷都不燃烧.请回答:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Fe Cu | B. | Cu | C. | Fe Ag | D. | Ag |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com