
| A. | 通过澄清的石灰水 | B. | 通过灼热的氧化铜 | ||
| C. | 通过炽热的炭 | D. | 点燃 |
分析 A、根据二氧化碳能够与石灰水反应,而一氧化碳不能分析;
B、根据一氧化碳可以还原灼热的氧化铜粉末,并生成二氧化碳,而二氧化碳不能与灼热的氧化铜反应分析;
C、根据灼热的炭会与二氧化碳生成一氧化碳进行分析;
D、二氧化碳气体中混有的少量一氧化碳气体,点燃不会燃烧.
解答 解:A、二氧化碳和氢氧化钙反应生成碳酸钙沉淀,混合气通过澄清石灰水后,会将二氧化碳吸收,但是二氧化碳是主要物质,故错误;
B、混合气通过灼热的氧化铜后,一氧化碳具有还原性,会转化成二氧化碳,最后就只剩下二氧化碳,故正确;
C、灼热的炭会与二氧化碳反应生成一氧化碳,但是一氧化碳是杂质,故错误;
D、虽然一氧化碳能燃烧,但由于二氧化碳气体中混有少量一氧化碳,二氧化碳不支持燃烧,所以根本就不能点燃一氧化碳,故错误.
故选:B.
点评 在解此类题时,首先分析杂质和物质的性质,然后选择适当的试剂只与杂质反应,不与主要物质反应,不会生成新的杂质.


科目:初中化学 来源: 题型:选择题
| A. | X的化学式是FeS2 | B. | SO2中的硫、氧元素的质量比为1:2 | ||
| C. | SO2中的硫、氧原子的个数比为1:2 | D. | Fe2O3中的铁元素的质量分数为70% |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 猜想1 | 猜想2 | 猜想3 |
| 只有CO | 只有CO2 | 含有CO和CO2 |

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 甲 | 乙 | 丙 | 丁 | |
| 反应前质量/g | 64 | 10 | 1 | 18 |
| 反应后质量/g | 0 | 54 | X | 2 |
| A. | 该反应属于分解反应 | |
| B. | 只有乙是生成物 | |
| C. | X等于36 | |
| D. | 该反应方程式中甲与丁的化学计量数之比为2:1 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
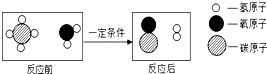
| A. | 该反应中含两种化合物 | B. | 水煤气的成分是一氧化碳和氧气 | ||
| C. | 该反应不符合质量守恒定律 | D. | 该反应中反应物的质量比为8:9 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com