取100g溶质质量分数为8%的氢氧化钠溶液,加入一定量溶质质量分数为20%的硫酸铜溶液,恰好完全反应,反应的化学方程式为CuSO4+2NaOH=Cu(OH)2↓+Na2SO4,求:
(1)反应生成沉淀的质量.
(2)反应后所得溶液中溶质的质量分数.(精确到0.1%)
【答案】
分析:(1)根据化学方程式,可以求出各物质间的质量比,并确定沉淀物为Cu(OH)
2;根据各物质之间的质量比,及已知物质NaOH和CuSO
4的质量,可计算求出反应生成沉淀的质量;
(2)由于其溶质应是反应后的生成物,而不是参与发应的事物,所以计算时应先算出反应后的溶质的质量,并确定溶液的总量,然后再根据溶质的质量分数公式计算.
解答:解:(1)设反应消耗的CuSO
4的质量为x,反应生成的Cu(OH)
2的质量为y,生成Na
2SO
4的质量为z,则
CuSO
4+2NaOH=Cu(OH)
2↓+Na
2SO
4160 80 98 142
x 100g×8% y z
∴
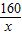
=
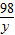
=
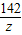
=
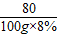
解之得:x=16g,y=9.8g,z=14.2g
故反应生成的沉淀的质量为9.8g;
(2)由(1)知CuSO
4的质量为16g,故硫酸铜溶液的质量为:16g÷20%=80g
∴反应后所得溶液中溶质的质量分数为:
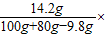
100%=8.3%
答:反应生成的沉淀的质量为9.8g;反应后所得溶液中溶质的质量分数为8.3%.
点评:本题主要考查学生根据化学方程式找出已知量和未知量的关系列比例式求解问题的能力及溶质质量分数的计算问题.根据化学方程式的计算,就是依据反应物和生成物间的质量比进行的;已知反应物的质量可以算出生成物的质量,反之,已知生成物的质量也可以算出所需反应物的质量.

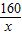 =
=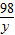 =
=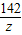 =
=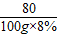
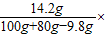 100%=8.3%
100%=8.3%

 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案