
| 56×3 |
| 56×3+16×4 |
| 374.7t |
| 500t |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
| A、-4 | B、-2 | C、+4 | D、+2 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 操作步骤 | 现象 | 结论 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、65:24 | B、24:65 |
| C、1:1 | D、无法确定 |
查看答案和解析>>
科目:初中化学 来源: 题型:
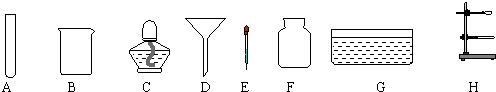
查看答案和解析>>
科目:初中化学 来源: 题型:
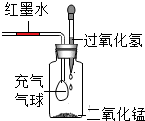
| A、气球胀大,红墨水左移 |
| B、气球缩小,红墨水左移 |
| C、气球胀大,红墨水右移 |
| D、气球缩小,红墨水右移 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验装置 | 实验主要过程 |
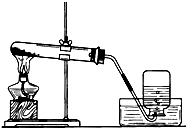 | a检查气密性:操作如下:先将导管伸入液面下,用手紧握试管,观察到 e检验气体,方法是 |
| 实验装置 | 实验主要过程 |
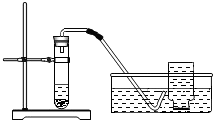 | a检查装置气密性:如何检查左图发生装置的气密性 |
查看答案和解析>>
科目:初中化学 来源: 题型:
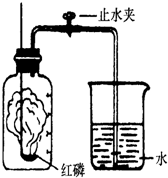 某同学设计了测定空气中氧气含量的实验,实验装置如图.
某同学设计了测定空气中氧气含量的实验,实验装置如图.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com