
| A. |  浓醋酸用做蓄电池 | B. |  硫酸用于生产染料 | ||
| C. |  盐酸用于除锈 | D. |  柠檬酸用于家庭自制汽水 |
科目:初中化学 来源: 题型:解答题
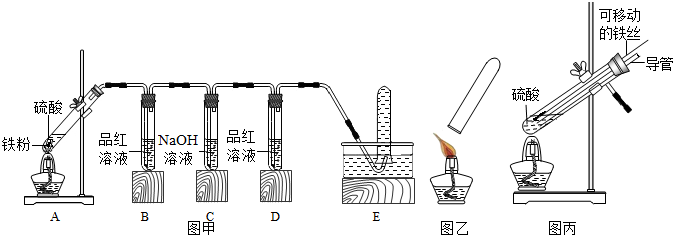
| A中硫酸浓度 | 实验现象 | A中生成气体成分 | |||
| B中品红溶液 | D中品红溶液 | 爆鸣实验 | |||
| 实验一 | 98% | 褪色 | 不褪色 | 无爆鸣声 | 只有SO2 |
| 实验二 | 45% | 稍有褪色 | 不褪色 | 有爆鸣声 | 有二氧化硫和氢气 |
| 实验三 | 25% | 不褪色 | 不褪色 | 有爆鸣声 | 只有H2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验.
某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ④①②⑤③ | B. | ②⑤④①③ | C. | ①②④⑤③ | D. | ④②⑤①③ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | 木条不复燃 | 常温下过氧氢溶液不分解 | |
| 实验二 | 在装有过氧化氢溶液的试管中加入少量FeCl3,然后将带火星的木条伸入试管中 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
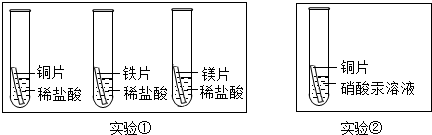
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com