
 ijУ��ѧ��ȤС��Ϊ�˲ⶨijһ̼������Ʒ��̼���Ƶ�������������������ʵ�飬ȡ13.25g̼������Ʒ�����ʼȲ�������Ҳ������ˮ�������ձ��У�����95.8gˮʹ����ȫ�ܽ⣬�������м���ϡ���ᣬ��÷�Ӧ�ų��������������������ϡ�����������ϵ������ͼ��ʾ����������������⣺
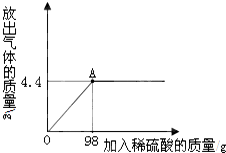
ijУ��ѧ��ȤС��Ϊ�˲ⶨijһ̼������Ʒ��̼���Ƶ�������������������ʵ�飬ȡ13.25g̼������Ʒ�����ʼȲ�������Ҳ������ˮ�������ձ��У�����95.8gˮʹ����ȫ�ܽ⣬�������м���ϡ���ᣬ��÷�Ӧ�ų��������������������ϡ�����������ϵ������ͼ��ʾ����������������⣺���� ��1����ͼ�ɿ���������98g�����Ƿ�Ӧǡ����ɣ�����4.4g������̼��������������ʱ������̼���������䣻
��2���ɸ��ݶ�����̼�����������û�ѧ����ʽ�����̼���Ƶ�������������������������
��� �⣺��1����ͼ�ɿ���������98g�����Ƿ�Ӧǡ����ɣ�����4.4g������̼��������������ʱ������̼���������䣬���Լ�������196g�����ɵĶ�����̼������Ҳ��4.4g��
��2������Ʒ��Na2CO3����Ϊx��
Na2CO3+H2SO4=Na2SO4+H2O+CO2��
106 142 44
x 4.4g
$\frac{106}{x}$=$\frac{44}{4.4g}$
x=10.6g
������Ʒ��̼���Ƶ���������Ϊ��$\frac{10.6g}{13.25g}$��100%=80%��
����Ʒ��̼���Ƶ���������Ϊ80%��
�ʴ�Ϊ����1��4.4��
��2��80%��
���� ������������״��㣬һ�Dz�����ȷ����ͼʾ���ݣ���һ�ʴ𰸼���Ϊ8.8g�����ǵ�����������Һ��������13.25��Ϊ̼���Ƶ�����ȥ��ѧ���ɲ��ս��������⣮


 �����Ļ���������人������ϵ�д�
�����Ļ���������人������ϵ�д� ���������ּ���ÿһ��ȫ�º�����ҵ��ϵ�д�
���������ּ���ÿһ��ȫ�º�����ҵ��ϵ�д� ��ٽ������½������������ϵ�д�
��ٽ������½������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  CO2���� | B�� |  �ռ�O2 | C�� |  �μ�Һ�� | D�� |  ����ҺpH ����ҺpH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
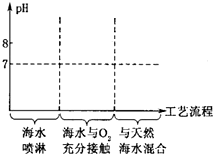 Ϊ�˼��������Σ�����ҹ��з��ˡ���ˮ�����������ա����乤�����̴����ǣ�
Ϊ�˼��������Σ�����ҹ��з��ˡ���ˮ�����������ա����乤�����̴����ǣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
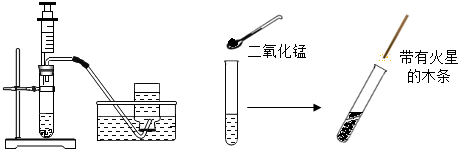
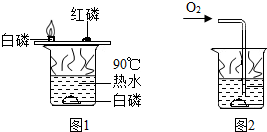 С����ͼ1��ʾװ��̽����ȼ��ȼ�յ���������������ˮ�еİ����ۻ���һ��ɫСҺ�Σ����ã�ͭƬ�İ���ʼȼ�գ�������ˮ�еİ�����ȼ�գ���ش�
С����ͼ1��ʾװ��̽����ȼ��ȼ�յ���������������ˮ�еİ����ۻ���һ��ɫСҺ�Σ����ã�ͭƬ�İ���ʼȼ�գ�������ˮ�еİ�����ȼ�գ���ش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
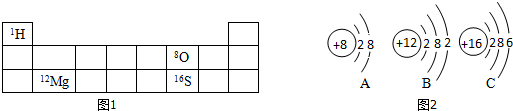
 ����
���� ����ʾ���ֲ�ͬ��ԭ�ӣ������ͼʾ�ش�
����ʾ���ֲ�ͬ��ԭ�ӣ������ͼʾ�ش�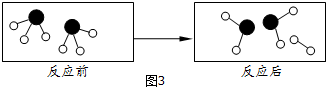
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
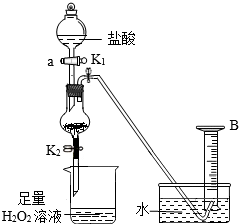 �Ȼ�����ʵ�����е���Ҫ�Լ���ijͬѧ��m g�������⣨Fe2O3���ķ���м����ȡFeCl3•6H2O���壬��FeCl3����H2O2�ֽ�Ĵ�����ͬʱ�ɲⶨ����м����������������Ϊ���������ͼװ�ã��г�װ���ԣ��������Ѽ��飩��
�Ȼ�����ʵ�����е���Ҫ�Լ���ijͬѧ��m g�������⣨Fe2O3���ķ���м����ȡFeCl3•6H2O���壬��FeCl3����H2O2�ֽ�Ĵ�����ͬʱ�ɲⶨ����м����������������Ϊ���������ͼװ�ã��г�װ���ԣ��������Ѽ��飩���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com