
һ�������£������Ϊ10 L���ܱ������У�1 mol A��1 mol B���з�Ӧ��
2A(g)��B(g) 2C(g)���ﵽƽ��ʱ����0.6 mol C������˵����ȷ���� ��������
2C(g)���ﵽƽ��ʱ����0.6 mol C������˵����ȷ���� ��������
A�����������ܶȱ��ֲ���ʱ�������жϷ�Ӧ�Ѵ�ƽ��
B�������������䣬�����������Ϊ5 L��C��ƽ��Ũ�ȱ�Ϊԭ����2��
C�������������䣬������ѹǿ��������A��ת���ʼ�С
D���ﵽƽ��ʱ��C������ٷֺ���Ϊ0.353

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
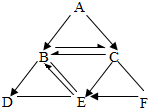 A��B��C��D��E��F����ѧ���ļ��ֻ�ѧ���ʣ�������һ�������µ�ת����ϵ��ͼ��ʾ������C�ڿ����к���ԼΪ21%�������������
A��B��C��D��E��F����ѧ���ļ��ֻ�ѧ���ʣ�������һ�������µ�ת����ϵ��ͼ��ʾ������C�ڿ����к���ԼΪ21%��������������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
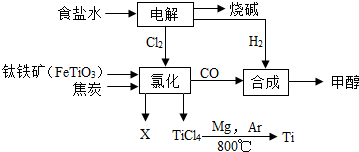 ��2013?�綫��ģ�⣩ij���ÿ���������ұ�������ȼ���״��������һ����ҵ������ͼ��ʾ��������������Դ�����ʣ������˻�����Ⱦ������д��
��2013?�綫��ģ�⣩ij���ÿ���������ұ�������ȼ���״��������һ����ҵ������ͼ��ʾ��������������Դ�����ʣ������˻�����Ⱦ������д��
| ||
| ||
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��60sʱZ��ƽ��Ũ��Ϊ0.03mol/L | B���������ݻ���Ϊ20L��Z����ƽ��Ũ�Ƚ�����ԭƽ��Ũ�ȵ�һ�� | C�����¶Ⱥ�������䣬������������1molX��Y��ת���ʽ����� | D���������¶ȣ�X�������������������Ӧ�ġ�H��0 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com