
分析 (1)氧化亚铜、铜都能够和硝酸反应生成硝酸铜;
氧化亚铜能和稀硫酸反应生成硫酸铜,铜不能和稀硫酸反应;
(2)铜在空气中高温灼烧时,能和空气中的氧气反应生成氧化铜;
(3)凡是有气体参加或产生的实验,实验前一定要检查装置的气密性,以防装置漏气影响实验结果;
反应产生的氢气中会含有少量水蒸气;
氢气和空气混合达到一定程度时,遇明火或加热时会发生爆炸;
碱石灰中含有氢氧化钠和氧化钙,能够吸收水蒸气和二氧化碳.
解答 解:(1)因为铜和氧化亚铜均可溶于稀硝酸形成蓝色溶液,所以方案1不合理;
因为氧化亚铜与稀硫酸反应能够生成Cu和Cu2+,导致溶液呈蓝色,所以方案2合理.
故填:方案1不合理,因为铜和氧化亚铜均可溶于稀硝酸形成蓝色溶液;方案2合理,因为氧化亚铜与稀硫酸反应能够生成Cu和Cu2+,导致溶液呈蓝色.
(2)设红色试样中含Cu的质量为x,
反应的氧气质量为:(c-a)-(b-a)=c-b,
灼烧过程中发生的反应为:4Cu+O2$\frac{\underline{\;灼烧\;}}{\;}$2Cu2O,
4Cu+O2$\frac{\underline{\;灼烧\;}}{\;}$2Cu2O,
256 32
x c-b
$\frac{256}{x}$=$\frac{32}{c-b}$,
x=8(c-b),
如有Cu2O,则8(c-b)<b-a,
即c<$\frac{9b-a}{8}$;
此实验方案至少要称量如下4次:干燥坩埚质量、坩埚加试样质量、灼烧后坩埚和药品总质量、再灼烧后坩埚和药品总质量(此次应与前一次相同方可,为重复实验,说明已加热至恒重).
故填:c<$\frac{9b-a}{8}$;4.
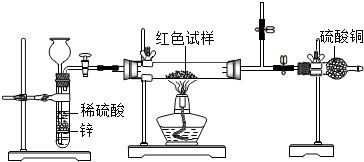
(3)检验气体发生装置气密性的方法是:关闭导气管上的活塞,从长颈漏斗中往试管中注水,长颈漏斗中的液面高度高于试管中的液面高度,一段时间液面高度保持不变,说明装置气密性良好.
故填:关闭导气管上的活塞,从长颈漏斗中往试管中注水,长颈漏斗中的液面高度高于试管中的液面高度,一段时间液面高度保持不变,说明装置气密性良好.
(4)A.在氢气发生器与硬质玻璃管之间加一个干燥装置,以防导出的氢气中含有的水蒸气影响实验结果;
B.加热前先排尽装置中的空气,以防发生爆炸,同时能够防止空气中的水蒸气影响实验结果;
C.在盛有硫酸铜的干燥管后再连接一个装有碱石灰的干燥管,以防空气中的水蒸气进入干燥管中影响实验结果.
故填:ABC.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.


科目:初中化学 来源: 题型:选择题
| A. | 不同种元素最本质的区别是质子数不同 | |
| B. | 打开啤酒瓶盖有大量气泡溢出,说明气体的溶解度和压强有关 | |
| C. | 用洗洁精洗餐具的原理是溶解 | |
| D. | 某合金可做保险丝,因该合金的熔点低 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 时间 | t1 | t2 | t3 | t4 | t5 |
| 生成气体的质量/g | 0.9 | 1.8 | 2.7 | 3.2 | 3.2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 实验结论 |
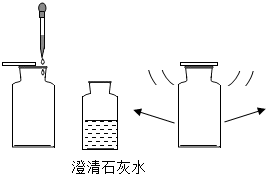 | 澄清石灰水变 浑浊 | 吸入的空气的二氧化碳含量比呼出的气体低 |
 | 燃着的小木条 熄灭 | 吸入的空气的氧气的含量比呼出的气体高 |
 | 干燥的玻璃片 出现水雾 | 吸入的空气的水蒸气含量比呼出的气体低 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Cu | B. | Zn | C. | Mg | D. | C |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 有腐蚀性的药液溅入眼睛内,要立即用水冲洗,切不可用手揉搓洒 | |
| B. | 稀酸飞溅到皮肤上,立即用大量的水冲洗,再涂上3%~5%的碳酸氢钠溶液 | |
| C. | 配制稀硫酸时,可先在量筒中加入一定量的浓硫酸,再慢慢注入水并不断搅拌 | |
| D. | 氢氧化钠溶液洒在衣服上,先用水冲洗后,再涂上硼酸溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①③⑥ | B. | ①④⑥ | C. | ②③⑥ | D. | ①⑤⑥ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 操作 | 现象 | 结论 | 化学方程式 | |
| (1) | 取少量溶液于试管中,滴加无色酚酞溶液 | 无色酚酞变红 | 溶液显碱性 | / |
| (2) | 取少量溶液于试管中,滴加稀盐酸 | 有气泡产生 | 溶液中存在碳酸根离子(或碳酸钠) | Na2CO3+2HCl═2NaCl+H2O+CO2↑; |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com