
【题目】完成下列基础的学生实验。
I.同学们利用如图所示装置进行气体的制备实验(A~E为装置编号)。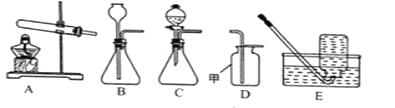
(1)写出图D装置中甲仪器的名称。
(2)用A装置加热氯酸钾和二氧化锰的混合物制取氧气,化学方程式为 , 其中二氧化锰起作用;收集氧气可以选择(填装置编号,下同)。
(3)实验室制取二氧化碳的化学方程式为 , 通常检验CO2气体的反应可用化学方程式表示为。
(4)常温下,可用固体硫化亚铁(FeS)和稀硫酸反应制取硫化氢(H2S)气体, 若要控制滴加液体的速率,可选择的发生装置是。
(5)实验室制取氢气选择的装置组合可以是。
(6)Ⅱ.根据“粗盐中难溶性杂质的去除”实验,回答有关问题。
实验步骤:
①溶解。称取5. 0g粗盐,逐渐加入10mL水中,直到不再溶解,剩余粗盐l.2g。
②过滤
③蒸发。请从溶解度的角度分析,实验中不采用降温结晶的方法得到精盐的依据是。
④计算产率。得到精盐3.2g,则精盐的产率为(计算结果保留一位小数)。
(7)整个实验中至少要进行次称量。
(8)从海水中获得的精盐,经过上述实验得到的精盐属于(填“混合物”或“纯净物“)。
【答案】
(1)集气瓶
(2)2KClO3 ![]() 2KCl+3O2 ↑,催化,D或E
2KCl+3O2 ↑,催化,D或E
(3)CaCO3 +2HCl=CaCl2 +H2O+CO2 ↑,Ca﹙OH﹚2 +CO2 =CaCO3 ↓+H2O
(4)C
(5)BE或CE
(6)氯化钠的溶解度受温度变化的影响小,84.2%
(7)2
(8)混合物
【解析】(1)图D装置中甲仪器的名称是集气瓶;
(2)用A装置加热氯酸钾和二氧化锰的混合物制取氧气,化学方程式为2KClO3 ![]() 2KCl+3O2 ↑,其中二氧化锰起催化作用;收集氧气可以选择D或E;
2KCl+3O2 ↑,其中二氧化锰起催化作用;收集氧气可以选择D或E;
(3)实验室制取二氧化碳的化学方程式为CaCO3 +2HCl=CaCl2 +H2O+CO2 ↑,通常检验CO2气体的反应可用化学方程式表示为Ca﹙OH﹚2 +CO2 =CaCO3 ↓+H2O;
(4)常温下,可用固体硫化亚铁(FeS)和稀硫酸反应制取硫化氢(H2S)气体,不需要加热,若要控制滴加液体的速率,可选择的发生装置是C;
(5)在实验室中用锌和稀硫酸反应制取氢气,属于固液常温型,所以应该选择B或C装置来制取氢气;氢气密度比空气小,难溶于水,所以应该选择E装置来收集氢气.
(6)③从溶解度的角度分析,实验中不采用降低溶液温度的方法得到精盐的依据是氯化钠的溶解度受温度的变化影响较小,相同情况下降温析出的晶体比较少;
④![]() ×100%=84.2%;
×100%=84.2%;
(7)最初所取粗盐的质量、剩余粗盐的质量(以此运用差量法得出溶解的粗盐的质量),以及所得精盐的质量,因此,最少需要3次称量;
(8)精盐中除了食盐,还有可溶性杂质,所以精盐属于混合物.
答案:(1)集气瓶;(2)2KClO3![]() 2KCl+3O2↑;催化; D或E;(3)CaCO3+2HCl=CaCl2+H2O+CO2↑;CO2+Ca(OH)2=CaCO3↓+H2O;(4)C;(5)BE或CE;(6)③氯化钠的溶解度受温度变化的影响小;④84.2%;(7)3;(8)混合物.
2KCl+3O2↑;催化; D或E;(3)CaCO3+2HCl=CaCl2+H2O+CO2↑;CO2+Ca(OH)2=CaCO3↓+H2O;(4)C;(5)BE或CE;(6)③氯化钠的溶解度受温度变化的影响小;④84.2%;(7)3;(8)混合物.
【考点精析】解答此题的关键在于理解催化剂的特点与催化作用的相关知识,掌握催化剂(触媒):在化学反应中能改变其他物质的化学反应速率,而本身的质量和化学性质在反应前后都没有发生变化的物质.(一变两不变)催化剂在化学反应中所起的作用叫催化作用,以及对二氧化碳的检验和验满的理解,了解验证方法:将制得的气体通入澄清的石灰水,如能浑浊,则是二氧化碳.验满方法:用点燃的木条,放在集气瓶口,木条熄灭.证明已集满二氧化碳气体.


科目:初中化学 来源: 题型:
【题目】给试管里的液体加热时,正确的操作是( )
A.试管内液体体积不超过试管容积的 1/2B.加热时直接对准药品部位加热
C.不可使试管口对着自己或旁人D.烧得很热的试管应立即用冷水冲洗干净
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有镁、铝两种金属分别与稀盐酸充分反应,生成相同质量氢气。某同学推测的情况如下:①足量的稀盐酸与等质量的镁、铝分别发生反应;②足量的稀盐酸与质量比为4∶3的镁、铝分别发生反应;③足量的稀盐酸与质量比为8∶9的镁、铝分别发生反应;④等质量、等溶质质量分数的稀盐酸与过量的镁、铝分别发生反应,其中正确的推测是( )
A. ①② B. ①④ C. ②④ D. ③④
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列矿石冶炼时产生的物质会污染空气且能形成酸雨的是( )
A.赤铁矿(Fe2O3)B.黄铁矿(FeS2)C.菱铁矿(FeCO3)D.磁铁矿(Fe3O4)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人们对空气污染程度的关注不断加强,我市也是空气污染比较严重的城市之一,气体①NO2②SO2③CO④CO2中能造成空气污染的是( )
A.①③③④B.②③④C.①②③D.①②
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列各说法中,不正确的是( )
A.增大可燃物与氧气的接触面积能促进可燃物的燃烧
B.依据质量守恒定律,镁条在氧气中燃烧前后,固体的质量不变
C.物质发生化学变化时,不仅有物质变化,还会伴随能量变化
D.分子、原子、离子都是构成物质的微观粒子
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】镁条在空气中久置表面会变黑。某小组同学设计并进行实验,探究镁条变黑的条件。
【查阅资料】常温下,亚硫酸钠(Na2SO3)可与O2发生化合反应。
【猜想与假设】常温下,镁条变黑可能与O2、CO2、水蒸气有关。
【进行实验】通过控制与镁条接触的物质,利用右图装置(镁条长度为3cm,试管容积为20mL),分别进行下列5个实验,并持续观察20天。
编号 | 主要实验操作 | 实验现象 |
① | 先充满用NaOH浓溶液洗涤过的空气 | 镁条始终无明显变化 |
② | 加入2mL NaOH浓溶液 | 镁条始终无明显变化 |
③ | 先加入2mL浓硫酸 | 镁条始终无明显变化 |
④ | 先加入4mL饱和Na2SO3溶液 | 镁条始终无明显变化 |
⑤ | 先加入2mL蒸馏水 | 镁条第3天开始变黑 |
【解释与结论】
(1)实验1和2中,NaOH浓溶液的作用是(用化学方程式表示)。
(2)实验1的目的是。
(3)实验3中,试管内的气体主要含有CO2、。
(4)得出“镁条变黑一定与CO2有关”结论,依据的两个实验是(填编号)。
(5)由上述实验可推知,镁条变黑的条件是。
(6)【反思与评价】
在猜想与假设时,同学们认为镁条变黑与N2无关,其理由是。
欲进一步证明镁条表面的黑色物质中含有碳酸盐,所需要的试剂是。
(7)【定量分析】小陆同学取了实验室存放较久的1克镁条和20克稀硫酸(足量)放入一支质量为30克的试管中,看到产生较多气泡,等没有气泡后精确称量,得到试管和内容物总质量为50.92克,小陆同学认为此反应产生的全部为氢气。试帮小陆同学计算这1 克镁条中还含有多少镁?
同学们经过讨论一致认为在操作和称量准确的情况下,实际含有的镁要小于计算结果。请你分析可以有原因
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com