
 Ęū³µŹĒĻÖ“śÉś»īÖŠ²»æÉȱɣµÄ“ś²½¹¤¾ß£®Ēė»Ų“šĻĀĮŠĪŹĢā?
Ęū³µŹĒĻÖ“śÉś»īÖŠ²»æÉȱɣµÄ“ś²½¹¤¾ß£®Ēė»Ų“šĻĀĮŠĪŹĢā?| CO |
| O2 |


 ĢŅĄīĪÄ»ÆæģĄÖŹī¼ŁĪäŗŗ³ö°ęÉēĻµĮŠ“š°ø
ĢŅĄīĪÄ»ÆæģĄÖŹī¼ŁĪäŗŗ³ö°ęÉēĻµĮŠ“š°ø ÓÅŠćÉśæģĄÖ¼ŁĘŚĆæŅ»ĢģČ«ŠĀŗ®¼Ł×÷Ņµ±¾ĻµĮŠ“š°ø
ÓÅŠćÉśæģĄÖ¼ŁĘŚĆæŅ»ĢģČ«ŠĀŗ®¼Ł×÷Ņµ±¾ĻµĮŠ“š°ø Źī¼Ł½ÓĮ¦ČüŠĀ½®ĒąÉŁÄź³ö°ęÉēĻµĮŠ“š°ø
Źī¼Ł½ÓĮ¦ČüŠĀ½®ĒąÉŁÄź³ö°ęÉēĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| ŹµŃéĻīÄæ | 1 | 2 | 3 | 4 |
| ¼ÓČėCaCl2ČÜŅŗÖŹĮæ | 50g | 100g | 150g | 200g |
| ²śÉś³ĮµķÖŹĮæ | 4g | 8g | 9g | 9g |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
 ³¬ŹŠĀōµÄ“æ¼īѳʷ֊ĶłĶłŗ¬ÓŠÉŁĮæµÄĀČ»ÆÄĘ£¬Ä³»ÆѧŠĖȤŠ”×éµÄĶ¬Ń§ĶعżŹµŃ饓²ā¶ØÄ³Ę·Åʵēæ¼īѳʷ֊Ģ¼ĖįÄʵÄÖŹĮæ·ÖŹż£®ĖūĆĒČ”ĮĖ5gøĆ“æ¼īѳʷ£¬ŌŚÉÕ±ÖŠÅäÖĘ³É60gČÜŅŗ£¬ŌŁĻņĘäÖŠÖšµĪ¼ÓČė10%µÄĀČ»ÆøĘČÜŅŗ£¬²āµĆ¼ÓČėĀČ»ÆøĘČÜŅŗµÄÖŹĮæÓė²śÉś³ĮµķµÄÖŹĮæ¹ŲĻµČēĶ¼ĖłŹ¾£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
³¬ŹŠĀōµÄ“æ¼īѳʷ֊ĶłĶłŗ¬ÓŠÉŁĮæµÄĀČ»ÆÄĘ£¬Ä³»ÆѧŠĖȤŠ”×éµÄĶ¬Ń§ĶعżŹµŃ饓²ā¶ØÄ³Ę·Åʵēæ¼īѳʷ֊Ģ¼ĖįÄʵÄÖŹĮæ·ÖŹż£®ĖūĆĒČ”ĮĖ5gøĆ“æ¼īѳʷ£¬ŌŚÉÕ±ÖŠÅäÖĘ³É60gČÜŅŗ£¬ŌŁĻņĘäÖŠÖšµĪ¼ÓČė10%µÄĀČ»ÆøĘČÜŅŗ£¬²āµĆ¼ÓČėĀČ»ÆøĘČÜŅŗµÄÖŹĮæÓė²śÉś³ĮµķµÄÖŹĮæ¹ŲĻµČēĶ¼ĖłŹ¾£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ

| 1 |
| 5 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
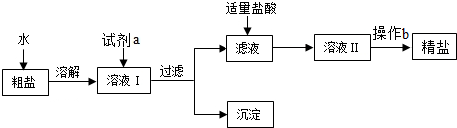
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
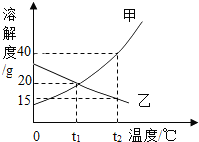 ¹ĢĢå¼×”¢ŅŅµÄČܽā¶ČĒśĻßČēĶ¼ĖłŹ¾£®
¹ĢĢå¼×”¢ŅŅµÄČܽā¶ČĒśĻßČēĶ¼ĖłŹ¾£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
 ”±ŗĶ”°
”±ŗĶ”° ”±·Ö±š±ķŹ¾Į½ÖÖ²»Ķ¬µÄŌ×Ó£¬øł¾ŻĶ¼Ź¾»Ų“šĻĀĮŠĪŹĢā£®
”±·Ö±š±ķŹ¾Į½ÖÖ²»Ķ¬µÄŌ×Ó£¬øł¾ŻĶ¼Ź¾»Ų“šĻĀĮŠĪŹĢā£®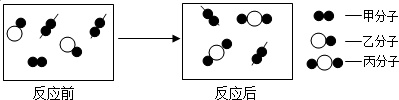
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢¹Æ-Ė®Ņų |
| B”¢Ńõ»ÆøĘ-ÉśŹÆ»Ņ |
| C”¢Ģ¼ĖįĒāÄĘ-“æ¼ī |
| D”¢ŅŅ“¼-¾Ę¾« |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com