
| A. | 金刚石用来裁玻璃 | B. | 焦炭用于炼铁 | ||
| C. | 干冰用作制冷剂 | D. | 石墨制铅笔芯 |
分析 物理性质是指物质不需要发生化学变化就表现出来的性质.化学性质是指物质在化学变化中表现出来的性质.而化学变化的本质特征是变化中有新物质生成,因此,判断物理性质还是化学性质的关键就是看表现物质的性质时是否有新物质产生.
解答 解:物质的颜色、状态、气味、熔点、沸点、硬度、密度等性质,不需要发生化学变化就表现出来,因此,都属于物理性质.
A、金刚石用来裁玻璃是利用金刚石的硬度大,利用了物理性质,故A错;
B、焦炭用于炼铁是利用焦炭的还原性,属于化学性质,故B正确;
C、干冰用作制冷剂是利用干冰升华吸热,使周围温度降低,没有新物质生成,利用了物理性质,故C错;
D、石墨制铅笔芯是利用石墨软,利用了物理性质,故D错.
故选B.
点评 物理性质、化学性质是一对与物理变化、化学变化有密切关系的概念,联系物理变化、化学变化来理解物理性质和化学性质,则掌握起来并不困难.


 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:初中化学 来源: 题型:选择题
| A. | 合金是由两种或两种以上金属熔合而成的具有金属特性的物质 | |
| B. | 铜的化学性质不活泼,所以铜制品不会生锈 | |
| C. | 在日常生活中,大量使用的常常不是纯金属,而是它们的合金 | |
| D. | “真金不怕火炼”说明黄金的硬度非常大 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 苏丹红 | B. | 硫磺 | C. | 硫酸铜 | D. | 三聚氰胺 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 镁条在空气中燃烧,发出耀眼白光,生成黑色固体 | |
| B. | 红磷在空气中燃烧,产生大量白烟 | |
| C. | 加热条件下,H2还原氧化铜,黑色粉末变成光亮红色 | |
| D. | 盐酸滴入Na2CO3粉末中,产生大量气泡 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
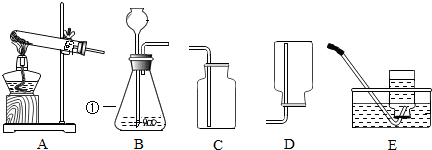
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
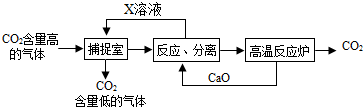 CO2是造成温室效应的主要气体,在工业上可用CO2来制备甲醇等物质.“碳捕捉技术”是指通过一定的方法,将工业生产中产生的CO2分离出来并利用,能有效地减少CO2气体的排放.如可利用NaOH溶液来“捕捉”CO2,其基本过程如图所示(部分条件及物质未标出).
CO2是造成温室效应的主要气体,在工业上可用CO2来制备甲醇等物质.“碳捕捉技术”是指通过一定的方法,将工业生产中产生的CO2分离出来并利用,能有效地减少CO2气体的排放.如可利用NaOH溶液来“捕捉”CO2,其基本过程如图所示(部分条件及物质未标出).查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com