
| 物质用途 | 金刚石切割玻璃 | 石墨作电极 |
| 对应性质 | ①硬度大 | ②导电性 |
| 1g物质完全燃烧 | 产生二氧化碳质量/g | 放出热量/kJ |
| 天然气 | 2.75 | 56 |
| 煤 | 3.67 | 32 |
分析 (1)物质的性质决定物质的用途,物质的用途反映物质的性质,根据常见的碳单质的性质和用途分析回答;
(2)根据常见的减缓“温室效应”的措施分析回答;
(3)根据化学方程式的书写方法分析回答.
(4)根基甲烷燃烧的反应写出反应的化学方程式.
(5)根据燃烧释放的热量和产生二氧化碳的量分析解答.
解答 解:(1)由于金刚石的硬度大,可用于切割玻璃等;由于石墨有优良的导电性,可用于作电极;由于活性炭有吸附性,可用于净水;故填:硬度大,导电性;
(2)减缓“温室效应”的措施很多,例如:大力植树造林,开发利用太阳能、风能等清洁能源;,故填:大力植树造林;
(3)在高温高压下,CO2和NH3可以合成尿素[CO(NH2)2],同时生成水.根据题意即可写出该反应的化学方程式为:CO2+2NH3$\frac{\underline{\;高温高压\;}}{\;}$CO(NH2)2+H2O.故填:CO2+2NH3$\frac{\underline{\;高温高压\;}}{\;}$CO(NH2)2+H2O.
(4)天然气中甲烷充分燃烧生成了二氧化碳和水,化学方程式为CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.故填:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
(5)根据表格提供的数据可以发现,天然气燃烧释放的热量多且产生的二氧化碳少,故填:释放的热量多且产生的二氧化碳少.
(6)由题意可知,4.4gCO2中碳元素质量=4.4g×$\frac{12}{44}$×100%=1.2g; 2.7gH2O中H元素质量=2.7g×$\frac{2}{18}$×100%=0.3g,由于碳氢元素的质量和是:1.2g+0.3g=1.7g<2.3g,则该物质中一定含有碳、氢、氧三种元素.可燃物中碳、氢元素质量比=1.2g:0.3g=4:1.故填:C、H、O,4:1.
点评 掌握常见的物质的性质和用途以及化学方程式的书写方法是正确解答本题的关键.


科目:初中化学 来源: 题型:解答题
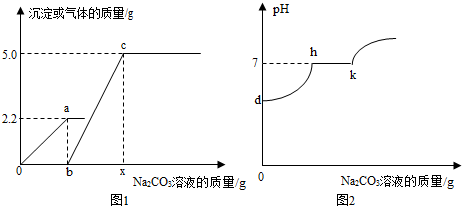
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
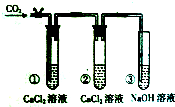 如图装置中,试管①②③里已分别盛有相应药品,向该装置中缓缓通入二氧化碳气体,经过一段时间后关闭止水夹,可能出现的现象是( )
如图装置中,试管①②③里已分别盛有相应药品,向该装置中缓缓通入二氧化碳气体,经过一段时间后关闭止水夹,可能出现的现象是( )| A. | 试管①中有沉淀产生 | B. | 试管②中有沉淀产生 | ||
| C. | 试管③中有沉淀产生 | D. | 试管①②③中均有沉淀产生 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
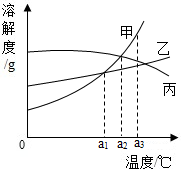
| A. | 把a1℃时甲、乙的饱和溶液升温到a2℃时仍是饱和溶液 | |
| B. | a2℃时,三种物质饱和溶液中溶质质量分数的大小关系为:甲=丙>乙 | |
| C. | 三种物质的溶解度都随温度的升高而增大 | |
| D. | a3℃时,三种物质的溶解度大小关系:甲>乙>丙 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 推广使用一次性筷子,减少疾病传染 | |
| B. | 废弃塑料可采用焚烧的方法处理,解决“白色污染” | |
| C. | 废旧金属的回收利用,保护金属资源 | |
| D. | 在农田中大量使用化肥、农药,以提高粮食产量 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com