
分析 (1)根据除了金、银等少数的化学性质非常稳定的金属,在自然界中能以单质形式存在外,其余均以化合物的形式存在,进行分析解答.
(2)根据镁能与空气中的氧气反应生成氧化镁,进行分析解答.
(3)Mg(OH)2固体加热分解为MgO和水;根据方程式的反应关系进行相关的计算及判断.
解答 解:(1)除了金、银等少数的化学性质非常稳定的金属,在自然界中能以单质形式存在外,其余均以化合物的形式存在,镁元素在自然界中是以化合物形式存在.
(2)镁能与空气中的氧气反应生成氧化镁,由工业制镁的反应原理,抽走容器中的空气对反应有促进作用,能防止空气中的氧气与Mg反应使产品混有氧化镁,氧化镁的化学式为:MgO.
(3)①Mg(OH)2固体加热分解为MgO和水,方程式为:Mg(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$MgO+H2O;
②由CaO+H2O═Ca(OH)2;Ca(OH)2+MgCl2═CaCl2+Mg(OH)2↓;Mg(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$MgO+H2O 可得MgO与MgCl2关系式为:MgCl2~MgO
设废液中含MgCl2的质量为x
MgCl2~MgO
95 40
x 4.0g
$\frac{95}{40}=\frac{x}{4.0g}$
x=9.5g
③由CaO+H2O═Ca(OH)2;Ca(OH)2+MgCl2═CaCl2+Mg(OH)2↓;可得CaO与MgCl2关系式为:MgCl2~CaO
设消耗氧化钙质量为y.
MgCl2~CaO
95 56
9.5g y
$\frac{95}{56}=\frac{9.5g}{y}$
y=5.6g
实际消耗8.4g CaO,说明废液中有过量的盐酸,发生了CaO+2HCl═CaCl2+H2O.
故答案为:(1)化合物;(2)MgO;(3)①Mg(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$MgO+H2O;②9.5;③Ca(OH)2+2HCl=CaCl2+2H2O(或CaO+2HCl=CaCl2+H2O).
点评 本题难度较大,考查海水资源的利用,学生应在物质转化中应学会利用化学方程式的计算来分析问题.


科目:初中化学 来源: 题型:选择题
| A. | 探究二氧化硫和水反应可能有硫酸生成 | |
| B. | 探究次氯酸钠( NaClO)和浓盐酸反应时会产生氮气 | |
| C. | 探究铜在酒精灯上灼烧时出现的黑色物质可能是炭黑 | |
| D. | 探究钠与水的反应产生的气体可能是氢气 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 食物、衣料和日常用品的丰富 | |
| B. | “神七”飞船从地球轨道转到月球轨道 | |
| C. | 新型材料的合成 | |
| D. | 化肥的合理使用 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
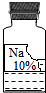 实验室有一瓶保存不当的试剂(如图所示),其残缺的标签中只剩下“Na”和“10%”字样,已知它是无色液体,是初中化学常用的试剂.小华等几位同学很感兴趣,决定对其成分进行探究.
实验室有一瓶保存不当的试剂(如图所示),其残缺的标签中只剩下“Na”和“10%”字样,已知它是无色液体,是初中化学常用的试剂.小华等几位同学很感兴趣,决定对其成分进行探究.| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 溶解度/g | 36 | 109 | 215 | 9.6 |
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取样品于试管中,滴加足量稀盐酸 | 有气泡冒出 | 猜想①正确,发生反应的化学方程式是Na2CO3+2HCl=2NaCl+H2O+CO2↑ |
| 步骤 | 现象 | 结论 |
| 步骤一:取样品于试管中,向其中滴加足量的CaCl2溶液并过滤 | 有白色沉淀生成 | 溶液中既含Na2CO3,又含有NaOH |
| 步骤二:向上述滤液中滴加酚酞试液 | 溶液变红色 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | +4 | B. | +3 | C. | +2 | D. | +1 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 紫色→红色→紫色 | B. | 紫色→蓝色→紫色 | C. | 紫色→红色→红色 | D. | 红色→紫色→红色 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 严禁用一只燃着的酒精灯去点燃另一只酒精灯 | |
| B. | 严禁向燃着的酒精灯添加酒精 | |
| C. | 用过的药匙,可以用纸擦也可以不擦 | |
| D. | 倾倒液体时,瓶盖要倒放,标签要向着手心 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com