
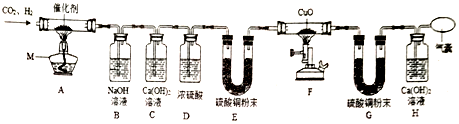
分析 (1)氢氧化钠能和二氧化碳反应生成碳酸钠和水,二氧化碳能使氢氧化钙溶液变浑浊,浓硫酸具有吸水性,可以用作某些气体的干燥剂;
根据反应物、生成物、反应条件及其质量守恒定律可以书写反应的化学方程式;
氢气具有还原性,加热条件下能和氧化铜反应生成铜和水;
(2)能量之间可以相互转化;
丙烷完全燃烧生成水和二氧化碳.
解答 解:(1)①装置A中发生反应的化学方程式为:CO2+4H2$\frac{\underline{催化剂}}{△}$CH4+2H2O.
故填:CO2+4H2$\frac{\underline{催化剂}}{△}$CH4+2H2O.
②B装置的作用除去从A装置排出的混合气体中的二氧化碳,C装置的作用是验证混合气体中CO2是否被除净.E装置的作用是验证混合气体中水是否被除净.
故填:验证混合气体中CO2是否被除净;验证混合气体中水是否被除净.
③装置G的作用是验证是否有水生成.
故填:验证是否有水生成.
④不同意他们的结论,理由是混合气体中的氢气未除去,氢气具有还原性,能和氧化铜反应生成铜和水,因此反应可能是氧化铜和氢气反应导致的.
故填:不同意;混合气体中的氢气未除去,氢气具有还原性,能和氧化铜反应生成铜和水.
(2)CH4燃料电池具有洁净、高效的特点,其工作时主要是将化学能转化为电能;
丙烷完全燃烧的化学方程式为:C3H8+5O2$\frac{\underline{\;点燃\;}}{\;}$4H2O+3CO2.
故填:化学;C3H8+5O2$\frac{\underline{\;点燃\;}}{\;}$4H2O+3CO2.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.


 金钥匙试卷系列答案
金钥匙试卷系列答案科目:初中化学 来源: 题型:选择题
 如表提供的四组物质符合如图所示相连物质在一定条件下可以发生反应的是( )
如表提供的四组物质符合如图所示相连物质在一定条件下可以发生反应的是( )| 甲 | 乙 | 丙 | 丁 | |
| A | NaOH | HCl | Cu | AgNO3 |
| B | CO2 | Ca(OH)2 | Na2CO3 | CaCl2 |
| C | KOH | BaCl2 | K2CO3 | HCl |
| D | CuSO4 | BaCl2 | Na2CO3 | Ba(OH)2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 加热时间/min | 0 | t1 | t2 | t3 |
| 固体质量/g | 2.94 | 2.46 | 1.98 | 1.98 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
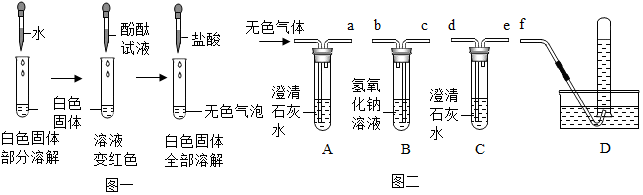
| 实验步骤 | 实验现象 | 实验结论 |
| 取氢氧化钙样品少量,研细后加适量蒸馏水 充分振荡后静置,向上层清液中滴加适量的酚酞试液. | 酚酞试液变红色. | 该样品还含有氢氧化钙 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
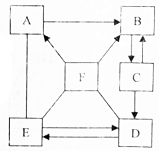 A-F都是初中化学中常见的物质,图中“-”表示相连的两种物质能发生化学反应,“→”表示相连的两种物质能转化(反应条件和部分反应物、生成物已省略).已知:D是现今产量最大的金属,其余物质均是化合物.A是胃液中含有的酸,B、C是由相同的两种元素组成的不同物质,常温下E为红色固体.
A-F都是初中化学中常见的物质,图中“-”表示相连的两种物质能发生化学反应,“→”表示相连的两种物质能转化(反应条件和部分反应物、生成物已省略).已知:D是现今产量最大的金属,其余物质均是化合物.A是胃液中含有的酸,B、C是由相同的两种元素组成的不同物质,常温下E为红色固体.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com