
| 实验操作 | 实验现象 | 实验结论 | |
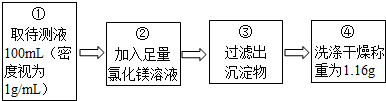
| 乙同学实验 | 取中和反应后的溶液少许于试管中,将表面反复打磨后的铝片放入试管的溶液中 | 铝片逐渐溶解,并有大量气泡冒出,收集气体点燃,火焰呈淡蓝色 | 猜想(2)成立 |
| 丙同学实验 | 取中和反应后的溶液少许于试管中,向试管中添加几滴无色酚酞试液 | 溶液变红色 | 猜想(3)成立 |
分析 氢氧化钠和稀盐酸反应生成氯化钠和水;
铝和稀盐酸反应生成氯化铝和氢气,和氢氧化钠溶液反应生成偏铝酸钠和氢气,氢气在空气中燃烧时发出淡蓝色火焰;
显碱性的溶液能使酚酞试液变红色.
解答 解:【做出猜想】
如果氢氧化钠恰好和稀盐酸完全反应,溶液中的溶质是氯化钠,如果氢氧化钠过量,溶质是氯化钠和氢氧化钠,如果稀盐酸过量,溶质是氯化钠和氯化氢.
故填:NaOH.
【小组讨论】
兴趣小组的同学讨论后发现不用做实验就可断定丁同学的猜想一定不正确,理由是氢氧化钠能与盐酸发生中和反应.
故填:丁;氢氧化钠能与盐酸发生中和反应.
【实验验证】
| 实验操作 | 实验现象 | 实验结论 | |
| 乙同学实验 | 取中和反应后的溶液少许于试管中,将表面反复打磨后的铝片放入试管的溶液中 | 铝片逐渐溶解,并有大量气泡冒出,收集气体点燃,火焰呈淡蓝色 | 猜想(2)成立 |
| 丙同学实验 | 取中和反应后的溶液少许于试管中,向试管中添加几滴无色酚酞试液 | 溶液变红色 | 猜想(3)成立 |
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:推断题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

| 实验操作 | 实验现象 | 实验结论 |
| 取少量钠的氧化物加入足量蒸馏水 | 猜想1正确 |
| 实验操作 | 实验现象 | 实验结论 |
| 1.取少量白色固体加入足量氯化钙溶液 | 产生白色沉淀 | 白色固体成分为Na2C03和 NaOH |
| 2.过滤、取少量滤液加入无色的酚酞试液 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
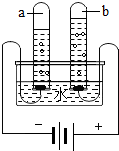 小华和小慧两位同学分别用如图所示的装置进行电解水实验.该反应的化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.为了增强水的导电性,实验前小华向水中加入硫酸钠固体.则b试管中产生的气体是O2(填化学式),检验这种气体的方法是带火星的木条.
小华和小慧两位同学分别用如图所示的装置进行电解水实验.该反应的化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.为了增强水的导电性,实验前小华向水中加入硫酸钠固体.则b试管中产生的气体是O2(填化学式),检验这种气体的方法是带火星的木条.| 实验操作 | 实验现象 | 实验结论 |
| ①取少量剩余溶液,滴入氯化铜溶液. | 产生蓝色絮状沉淀 | 溶液中含有氢氧化钠 |
| ②将①中反应后混合物过滤,向滤液中加入足量稀硝酸再滴入几滴硝酸银溶液 | 产生白色沉淀 | 溶液中含有氯化钠 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
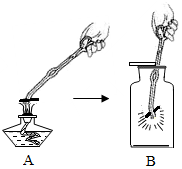 今年5月我市九年级学生进行了化学实验操作考试,考到了“木炭在氧气中燃烧”这一实验,如图所示,请回答:
今年5月我市九年级学生进行了化学实验操作考试,考到了“木炭在氧气中燃烧”这一实验,如图所示,请回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com