
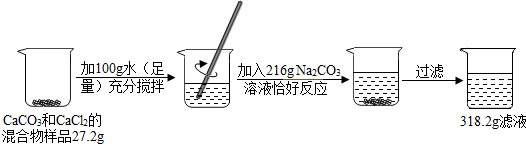
分析 (1)根据质量守恒定律可计算出过滤所得碳酸钙的质量,依据化学反应中元素守恒即可解答;
(2)首先根据氯化钙转化为碳酸钙时质量差计算出氯化钙的质量;
(3)根据化学方程式可计算出所得滤液的溶质氯化钠的质量,再依据溶质质量分数计算公式即可解答.
解答 解:(1)过滤所得碳酸钙的质量:27.2g+100g+216g-318.2g=25g;
钙元素的质量:25g×$\frac{40}{40+12+16×3}×100%$=10g;
原固体混合物中钙元素的质量分数:$\frac{10}{27.2g}×100%$=36.8%;
(2)设原固体混合物中氯化钙的质量为x,
CaCl2→CaCO3↓ 质量减少
111 100 111-100=11
x 27.2g-25g=2.2g
则$\frac{111}{x}=\frac{11}{2.2g}$,解得:x=22.2g
(3)设过滤所得滤液的溶质氯化钠的质量为y,
CaCl2+Na2CO3=CaCO3↓+2NaCl
111 117
22.2g y
则$\frac{111}{22.2g}=\frac{117}{y}$,解得y=23.4g
最终过滤所得滤液的溶质质量分数是:$\frac{23.4g}{318.2g}×100%$=7.4%;
故答案为:
(1)36.8%;(2)22.2g;(3)7.4%.
点评 主要考查学生对完全反应的认识,以及运用化学方程式和溶质质量分数公式进行计算的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 不同的酸具有相似的化学性质是因为酸溶液中有大量的H+ | |
| B. | 不同的碱具有相似的化学性质是因为碱溶液中有大量的OH- | |
| C. | 硫酸铜、氯化铜溶液都呈蓝色,是因为它们的溶液都含有Cu2+ | |
| D. | 浓盐酸具有挥发性,而浓硫酸无挥发性,是因为溶液中溶质质量分数不同 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验方案 | 实现现象 | 结论 |
| ①取一定量的合金粉末,加过量的30%的氢氧化钠溶液 30%的氢氧化钠溶液,充分反应后过滤,滤渣备用. | 粉末部分溶解,并有气体放出. | 合金中一定含有铝. |
| ②取步骤①所得滤渣,加过量的 10%盐酸,充分反应. | 滤渣部分溶解,并有气体放出,溶液呈浅绿色. | 合金中一定含有铁和铜. |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①②③ | B. | ④⑤⑥ | C. | ①③⑤ | D. | 都不正确 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
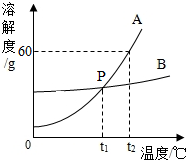 小聪同学绘制了如图A、B两种固体物质的溶解度曲线.
小聪同学绘制了如图A、B两种固体物质的溶解度曲线.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com