

分析 根据掌握的常见气体的性质和鉴别方法进行综合实验的分析验证,过程中要分析命题人的设计意图,也就是根据设计原理进行分析和评价.
解答 解:【实验猜想】由于猜想1:只有CO和猜想3:含有CO和CO2;所以猜想2:只有 CO2;
【实验探究】
(1)观察到A装置中的澄清石灰水变浑浊,证明草酸分解有CO2气体生成,装置中是氢氧化钙和二氧化碳反应生成碳酸钙和水,对应的化学反应方程式:CO2+Ca(OH)2=CaCO3↓+H2O;
(2)有两种实验现象都能分别证明草酸分解的气体中含有CO:
①当有一氧化碳时,由于一氧化碳具有还原性而转化为二氧化碳,所以对应的现象为C装置澄清石灰水不变浑浊,F装置中出现 变浑浊的现象;
②当有一氧化碳时,由于一氧化碳具有还原性而夺取氧化铜中的氧元素使氧化铜转化为铜,所以对应的现象为E装置中出现黑色粉末变成红色的现象.
【实验结论】通过实验探究证明:猜想3成立.
草酸分解生成水、一氧化碳和二氧化碳,对应的化学方程式为 H2C2O4$\frac{\underline{\;\;△\;\;}}{\;}$H2O+CO↑+CO2↑.
【问题讨论】
(1)氢氧化钙溶解度小,但是与二氧化碳反应有明显的现象就是生成白色沉淀,所以B装置的作用是检验二氧化碳;
(2)氢氧化钠的溶解度大,利于用来吸收二氧化碳,所以C装置的作用是 吸收二氧化碳;
(3)由于一氧化碳有毒,所以该试验装置的设计还有一处明显不足(实验前已排尽装置内的空气),请提出改进措施 点燃尾气或者收集尾气(任写一条).
故答案为:
【实验猜想】CO2;
【实验探究】
(1)CO2+Ca(OH)2=CaCO3↓+H2O;
(2)
①变浑浊;
②黑色粉末变成红色.
【实验结论】H2C2O4$\frac{\underline{\;\;△\;\;}}{\;}$H2O+CO↑+CO2↑.
【问题讨论】
(1)除去二氧化碳;
(2)检验二氧化碳是否除尽;
(3)点燃尾气或者收集尾气.
点评 熟悉常见气体的制备原理以及对应的化学方程式,对应的制取与收集装置等,实验中的注意事项要注意意义对应.


 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:初中化学 来源: 题型:填空题
 如图是同学们在实验室制作叶脉书签的部分操作步骤.请回答:
如图是同学们在实验室制作叶脉书签的部分操作步骤.请回答:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 ”和“
”和“ ”表示两种不同的原子.
”表示两种不同的原子.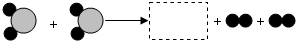
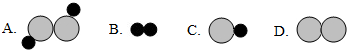
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
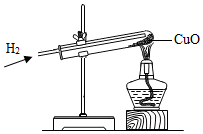 将氢气通入盛有氧化铜的试管中,加热一段时间后,可观察到试管中有红色固体出现.
将氢气通入盛有氧化铜的试管中,加热一段时间后,可观察到试管中有红色固体出现.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
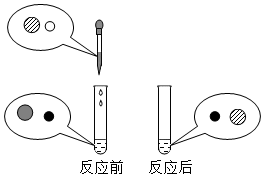 向氢氧化钠溶液中滴加稀盐酸至恰好完全反应,反应前后溶液中存在的离子种类如图所示(其中“〇”“
向氢氧化钠溶液中滴加稀盐酸至恰好完全反应,反应前后溶液中存在的离子种类如图所示(其中“〇”“ ”表示不同离子).则下列说法正确的是( )
”表示不同离子).则下列说法正确的是( )| A. | 〇表示氯离子 | |
| B. |  表示钠离子 表示钠离子 | |
| C. |  可用适量硝酸银溶液和足量稀硝酸进行检测 可用适量硝酸银溶液和足量稀硝酸进行检测 | |
| D. | 此反应的实质是 和〇结合生成水分子 和〇结合生成水分子 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
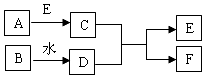 如图中A~F分别表示一种常见化合物,A、B都是氧化物,A通常为气态,F常用于实验室制取A(部分生成物已略去).
如图中A~F分别表示一种常见化合物,A、B都是氧化物,A通常为气态,F常用于实验室制取A(部分生成物已略去).查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 小明在市场看到,鱼老板将一勺白色粉末加入水中,水中奄奄一息的鱼很快张开嘴,活蹦乱跳起来,小明对这种“白色粉末”很感兴趣,与小刚进行了相关探究.
小明在市场看到,鱼老板将一勺白色粉末加入水中,水中奄奄一息的鱼很快张开嘴,活蹦乱跳起来,小明对这种“白色粉末”很感兴趣,与小刚进行了相关探究.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 在化学反应前后,物质所含元素化合价发生变化的反应属于氧化还原反应.氧化还原反应与四种基本反应类型间的关系如图所示,下列举例中错误的是( )
在化学反应前后,物质所含元素化合价发生变化的反应属于氧化还原反应.氧化还原反应与四种基本反应类型间的关系如图所示,下列举例中错误的是( )| A. | 例1:C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2 | B. | 例2:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑ | ||
| C. | 例3:Mg(OH)2+2HCl═MgCl2+2H2O | D. | 例4:Cu+2AgNO3═2Ag+Cu(NO3)2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com