
| 选项 | 物质 | 杂质 | 除去杂质的方法 |
| A | N2 | O2 | 通过灼热的铜网 |
| B | KCl | MnO2 | 加水充分溶解,过滤,蒸发结晶 |
| C | FeSO4溶液 | CuSO4 | 加入足量锌粉,充分反应,过滤 |
| D | NaCl溶液 | CaCl2 | 滴加碳酸钠溶液至恰好完全反应,过滤 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、氧气通过灼热的铜网时可与铜发生反应生成氧化铜,而氮气不与铜反应,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
B、KCl易溶于水,MnO2难溶于水,可采取加水溶解、过滤、蒸发结晶的方法进行分离除杂,故选项所采取的方法正确.
C、FeSO4溶液和CuSO4均能与足量锌粉反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
D、CaCl2能与碳酸钠溶液反应生成碳酸钙沉淀和氯化钠,至恰好完全反应,过滤,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
故选:C.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
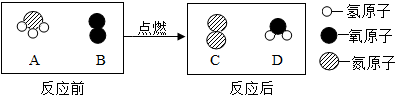
| A. | 该反应中有两种化合物分子 | |
| B. | 该反应中,参加反应的A、B分子的个数比为4:3 | |
| C. | 物质C的化学性质不活泼,常用作保护气 | |
| D. | 在该反应中,生成C和D的质量比为14:9 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 实验操作 | 现象 | 结论 | |
| A | 向收集满CO2的软塑料瓶中加入约$\frac{1}{3}$体积的NaOH溶液,旋紧瓶盖,振荡 | 塑料瓶变瘪 | CO2能与NaOH反应 |
| B | 向某白色粉末中滴加适量稀盐酸 | 白色粉末消失,产生气泡 | 白色粉末是Na2CO3 |
| C | 向稀盐酸与NaOH溶液反应后的试管中滴加无色酚酞 | 溶液无明显现象 | 恰好完全反应 |
| D | 点燃从导管放出的某气体,在火焰上方罩一个冷而干燥的烧杯 | 烧杯内壁有无色液滴产生 | 该气体中含氢元素 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 加热氢氧化铜悬浊液,产生紫红色固体 | |
| B. | 木炭在空气中剧烈燃烧,发出耀眼白光 | |
| C. | 点燃棉纱线,产生烧焦羽毛气味 | |
| D. | 聚乙烯塑料加热时熔化,冷却后变成固体 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 在工业上,碳酸钠广泛用于玻璃、造纸、纺织和洗涤剂的生产等.
在工业上,碳酸钠广泛用于玻璃、造纸、纺织和洗涤剂的生产等.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 :表示为Cl-;
:表示为Cl-; 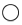 :表示为H+;
:表示为H+;  :表示为Fe2+.
:表示为Fe2+.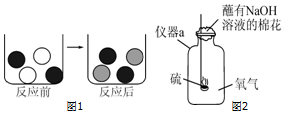
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
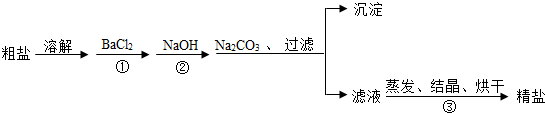
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 碱石灰有吸水性,可干燥SO2 | |
| B. | CO2不可燃,可扑灭燃着的镁带 | |
| C. | 氢氧化钠是碱,可改良酸性土壤 | |
| D. | 硫酸铜能使蛋白质变性,可用于游泳池水消毒 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com