
| 温度 物质 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 |
| Na2CO3 | 7.0 | 12.5 | 21.5 | 39.0 | 49.0 |
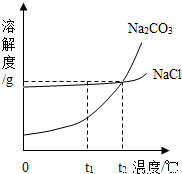
| 温度 物质 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 |
| Na2CO3 | 7.0 | 12.5 | 21.5 | 39.0 | 49.0 |
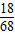 ×100%=26.5%;若使其中的氯化钠完全溶解,所采取的最有效的措施是加水.
×100%=26.5%;若使其中的氯化钠完全溶解,所采取的最有效的措施是加水.

科目:初中化学 来源: 题型:
(2013?门头沟区一模)某同学为研究氢氧化钠溶液与稀盐酸是否恰好中和时,取少量反应后的溶液于试管中,分别用不同试剂进行实验.下列实验方法及结论不正确的是( )
|
查看答案和解析>>
科目:初中化学 来源: 题型:



| 实验操作 | 实验结果 |
| 取100mL水,加入25gKNO3,搅拌,20℃ | 全部溶解,得溶液① |
| 再加Xg KNO3,搅拌,20℃ | 恰好饱和,得溶液② |
| 再加25g KNO3,搅拌,20℃ | 得溶液③ |
| 加热 | 全部溶解,得溶液④ |
| 冷却至20℃ | 晶体析出,得溶液⑤ |
查看答案和解析>>
科目:初中化学 来源: 题型:
 (2013?门头沟区一模)某化学小组在课外活动时做了一个实验,在甲试管中装入固体物质,乙试管中装入液体试剂,按如图所示组装好仪器(图中铁架台等仪器已略去).
(2013?门头沟区一模)某化学小组在课外活动时做了一个实验,在甲试管中装入固体物质,乙试管中装入液体试剂,按如图所示组装好仪器(图中铁架台等仪器已略去).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com