
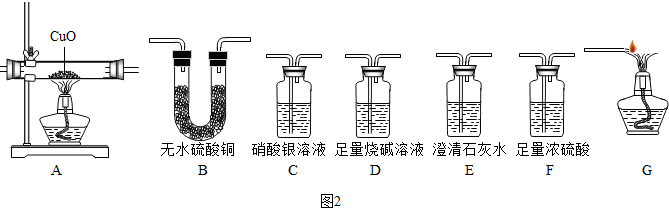
分析 首先要明确每一个装置的作用,通过灼热的氧化铜来证明是否含有还原性气体(如氢气和一氧化碳等),通过无水硫酸铜来证明水分,硝酸银溶液用来检验氯化氢气体,烧碱溶液(氢氧化钠溶液)一般用来除去酸性气体(二氧化碳、氯化氢等),石灰水用来检验二氧化碳,浓硫酸用来吸收水分;多个装置进行组合时,要根据实验要求正确的按顺序连接,以排除可能造成的干扰.
解答 解:要验证混合气体由HCl、H2、CO三种气体组成,要先检验HCl气体,可选用硝酸银溶液(若含有氯化氢气体,会产生白色沉淀);最后验证混合气体由H2、CO,方法是检验它们和氧化铜反应后是否生成水和二氧化碳,要排除二氧化碳的干扰,故要先除去二氧化碳,并干燥,反应后为了排除气体通过石灰水可能带出水蒸气的干扰,混合气体通过氧化铜后要先通过无水硫酸铜,再通入澄清的石灰水检验有无二氧化碳生成.
装置D中:烧碱溶液(氢氧化钠溶液)一般用来除去酸性气体(二氧化碳、氯化氢等),若无该装置,A装置的实验无法进行;
装置F:如果没有F装置,无法排除水蒸气的干扰,无法证明有无氢气存在;
装置D:一氧化碳有毒,能造成空气污染,所以需要处理含一氧化碳的尾气.
故答案为:BCDFABE;无法验证H2、CO的存在;无法证明有无氢气存在:处理含一氧化碳的尾气.
点评 本题难度不是很大,是中考的重要考点之一,熟练掌握常见气体的检验与除杂方法等是正确解答本题的关键.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:选择题
| A. | 用滤纸过滤可以降低水的硬度 | |
| B. | 用肥皂水可以区分硬水和软水 | |
| C. | 为了保护水资源,禁止使用化肥和农药 | |
| D. | 电解水时,负极端的玻璃管中产生的气体能使带火星的木条复燃 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2 溶液 |
| 实验操作 |  |  | 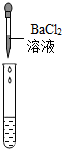 |
| 实验现象 | 试纸变色,比照比色卡,pH<7 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中只有H2SO4 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com