
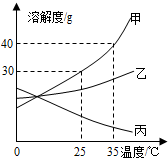
 甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答:
甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答:分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)25℃时,甲物质的溶解度30g即100g水中最多溶30g,则50g水中最多溶15g,所得溶液质量为:15g+50g=65g;
(2)如果溶解度受温度影响较大的物质从溶液中结晶析出的方法是冷却热饱和溶液,如果溶解度受温度影响不大的物质从溶液中结晶析出的方法是蒸发溶剂.因为甲的溶解度随温度影响较大,所以用降温结晶的方法,具体步骤是:溶解,加热浓缩制成饱和溶液,再降温,析出晶体后过滤;
(3)将35℃时丙的饱和溶液降温到25℃,丙的溶解度变大,溶液由饱和变为不饱和,没有晶体析出,故溶质质量分数不变;
(4)因为甲的溶解度随温度的升高而增大,所以开始发现全部溶解,一段时间后又有部分甲的晶体析出说明开始物质溶于水放热,温度升高,溶解度增大,冷却后溶液温度降低,溶解度变小,所以析出晶体.
故答案为:(1)65;
(2)adcb;
(3)不变;
(4)甲固体溶于水时放热.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.


科目:初中化学 来源: 题型:填空题
 如表是Ca(OH)2和NaOH的溶解度数据.请回答下列问题:
如表是Ca(OH)2和NaOH的溶解度数据.请回答下列问题:| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
| NaOH | 31 | 91 | 111 | 129 | 313 | 336 | |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 滤渣是Ag、Cu、Fe | B. | 滤液中有Zn2+、Fe2+、NO3- | ||
| C. | 滤渣是Zn、Cu、Ag | D. | 金属活动性顺序为Ag<Cu<Fe<Zn |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 烧杯+盐酸 | 大理石 | 充分反应后烧杯+剩余物 | |
| 甲 | 75.0g | 12g | 82.6g |
| 乙 | 75.0g | 16.0g | 86.6g |
| 丙 | 95.0g | 12g | 102.6g |
查看答案和解析>>
科目:初中化学 来源:2017届湖北省九年级下学期第二次月考化学试卷(解析版) 题型:探究题
化学兴趣小组中某同学表演了“水能生火”的魔术。他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来。小李很感兴趣,于是,他和同学们进行探究。
【提出问题】过氧化钠与水反应生成了什么物质?为什么脱脂棉会燃烧?
【猜想】①可能有一种气体和另一种物质生成 ②反应过程中可能有热量放出
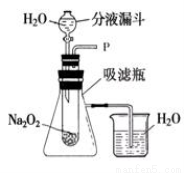
【实验装置】如图所示:
【实验探究】
实验一:探究反应后生成的气体是什么?
①打开如图装置中分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃。说明生成的气体是:_________________
②实验中,还观察到伸入烧杯中的导管口有气泡冒出。
实验二:继续探究反应后生成的另一种物质是什么?
①小张猜想另一种物质是Na2CO3,小李认为不可能。小李的依据是___________。
②小李取反应后所得的溶液于试管中,滴入无色酚酞试液,发现酚酞试液变红色。说明反应后所得的溶液呈____________性。
【表达】由实验探究的结果,写出过氧化钠和水反应的化学方程式_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com