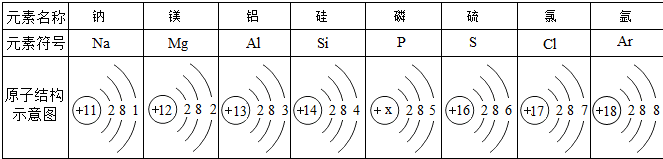
某校化学兴趣小组参观制碱厂后,获得以下信息并对相关问题进行研究.
【产品与原理】该厂采用“侯氏制碱法”生产化工产品--纯碱(Na
2CO
3)和化肥NH
4Cl.
生产原理是:将NH
3和CO
2通入饱和食盐水中得到NaHCO
3和NH
4Cl的混合物,反应为:NaCl(饱和)+NH
3+CO
2+H
2O═NaHCO
3↓+NH
4Cl;分离出NaHCO
3,加热制得纯碱.
【生产流程】
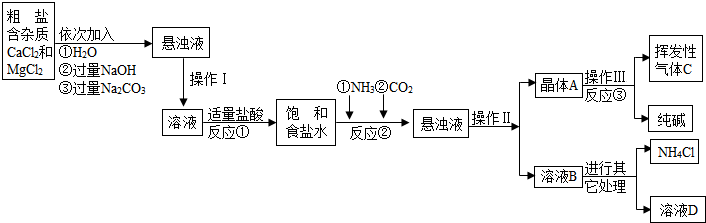
【相关资料】
(1)NH
4Cl
NH
3↑+HCl↑
(2)已知20℃时有关物质的溶解度如下(气体指1体积水中能溶解的气体体积)
| 物质 |
NaCl |
NaHCO3 |
NH4Cl |
NH3 |
CO2 |
| 溶解度 |
36.0g |
9.6g |
37.2g |
710 |
0.9 |
【问题讨论】:
(1)氨碱工业最关键的一步是:在加压的条件下不断向饱和的氨盐水中通入二氧化碳气体,溶液中会有碳酸氢钠晶体析出.试分析该流程需要加压条件的原因是:
.
(2)反应①中发生了两个反应,写出其中的一个化学方程式:
.
(3)反应③中得到纯碱的化学方程式为:
.
(4)溶液B中的溶质有
(至少写出两种).
(5)上述生产流程中可循环使用的是
(填序号).
A.挥发性气体C B.溶液D C.氢氧化镁 D.化肥NH
4Cl
(6)在氨碱工业处理剩余的氯化铵溶液时.为何不直接蒸发结晶析出氯化铵固体?
.
【组成确定】
(1)称取一定质量的纯碱样品,经多次充分加热后,再称重,质量无变化;
(2)另取少量纯碱样品加入适量水,样品完全溶解,向该溶液中加入过量稀HNO
3,再滴加AgNO
3溶液,有白色沉淀.由上述实验可确定纯碱样品含有杂质
(写化学式).
(3)某研究性学习小组对刚生产出的纯碱产品进行检测.取22克该样品于烧杯中,加水将其溶解,然后逐滴加入溶质质量分数为14.6%的稀盐酸并不断振荡.
首先发生的反应是:Na
2CO
3+HCl═NaHCO
3+NaCl;
然后发生的反应是:NaHCO
3+HCl═NaCl+H
2O+CO
2↑;
在上述过程中烧杯中溶液质量与加入稀盐酸质量的关系如图甲所示.
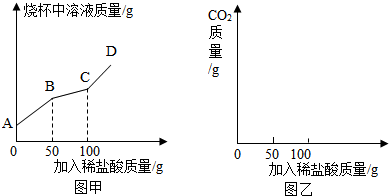
①请你根据图甲提供的信息,在图乙的坐标系中画出检测过程中产生CO
2的质量随滴加盐酸质量的变化曲线.(标明二氧化碳质量的相应数值)
②计算该样品中纯碱的质量分数.(计算结果用百分数表示,保留到小数点后一位)