
| 选项 | 物质(杂质) | 操作方式 |
| A | Cu(Fe) | 加足量稀硫酸,充分反应后过滤 |
| B | CO(O2) | 缓慢通过灼热铜网 |
| C | NaCl溶液(Na2CO3) | 加盐酸至恰好不再产生气泡为止 |
| D | FeSO4溶液(CuSO4) | 加入足量铁屑,充分反应后过滤 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、Fe能与稀硫酸反应生成硫酸亚铁溶液和氢气,铜不与稀硫酸反应,充分反应后过滤,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
B、一氧化碳与氧气的混合气体在通过灼热铜网时易发生爆炸,不符合除杂原则,故选项所采取的方法错误.
C、Na2CO3能与盐酸反应生成氯化钠、水和二氧化碳,至恰好不再产生气泡为止,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
D、足量铁屑能与CuSO4溶液反应生成硫酸亚铁溶液和铜,充分反应后过滤,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
故选:B.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.


科目:初中化学 来源: 题型:选择题
| A. | 催化剂只能改变化学反应的速率,而不能增加生成物的产量 | |
| B. | 不加入二氧化锰,过氧化氢也能分解产生氧气 | |
| C. | 生物体中化学反应几乎都是在酶的催化作用下进行的 | |
| D. | 催化剂只能加快其他物质的化学反应速率而本身质量不变 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解 度/g | NaCl | 35.7 | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 |
| KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
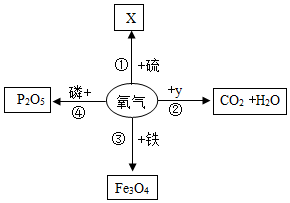 氧气能与许多物质发生反应.小明同学学习了之后进行了如图整理.(部分反应条件已略去).
氧气能与许多物质发生反应.小明同学学习了之后进行了如图整理.(部分反应条件已略去).查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 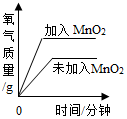 两份等质量、等溶质质量分数的双氧水溶液在有无MnO2的情况下产生 两份等质量、等溶质质量分数的双氧水溶液在有无MnO2的情况下产生 | |
| B. | 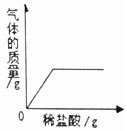 向部分变质的氢氧化钠溶液中滴加稀盐酸 向部分变质的氢氧化钠溶液中滴加稀盐酸 | |
| C. | 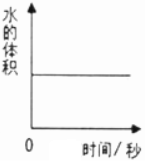 用燃磷法测定空气中氧气的含量 用燃磷法测定空气中氧气的含量 | |
| D. | 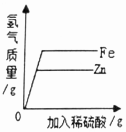 向等质量的铁、锌中分别加入稀硫酸 向等质量的铁、锌中分别加入稀硫酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com