
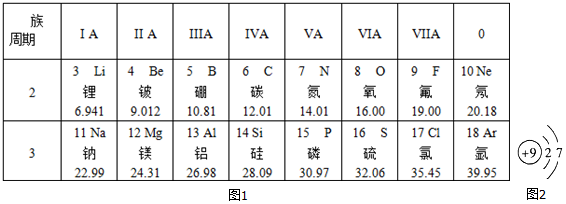
分析 (1)根据元素周期表的信息来分析;
(2)根据元素的分类以及离子符号的写法来分析;
(3)第11号元素与第17号元素分别是钠元素和氯元素,组成的化合物是氯化钠,据此进行分析解答;
(4)根据元素是质子数(即核电荷数)相同的一类原子的总称,决定元素种类的是质子数(即核电荷数),据此进行分析解答;
(5)根据原子结构示意图的信息以及最外层电子数来分析.
解答 解:(1)第2周期第ⅢA族元素是硼,其元素符号为B;故填:B;
(2)第3周期中的金属元素钠、镁、铝,钠原子易失去一个电子而形成带一个单位正电荷的钠离子;镁原子易失去2个电子而形成带2个单位正电荷的镁离子;铝原子易失去3个电子而形成带3个单位正电荷的铝离子;故填:钠(或镁或铝);Na+(或Mg2+或Al3+);
(3)第11号元素与第17号元素分别是钠元素和氯元素,组成的化合物是氯化钠;氯化钠是由钠离子和氯离子构成的;故填:NaCl;离子;
(4)元素是质子数(即核电荷数)相同的一类原子的总称,决定元素种类的是质子数(即核电荷数),不同种元素最本质的区别是质子数(即核电荷数)不同;故填:质子数(即核电荷数)不同;
(5)由9号元素的原子结构示意图可知,其最外层有7个电子,在化学反应中易得到电子;故填:7;得.
点评 本题难度不大,考查学生灵活运用元素周期表中元素的信息、常见物质的粒子构成等进行分析解题的能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:选择题
| A. | 用后的滴管平放在实验桌上 | |
| B. | 药品直接放在托盘上称量 | |
| C. | 试剂瓶塞正放在实验台上 | |
| D. | 滴瓶上的滴管用后不用水冲洗直接放回滴瓶 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
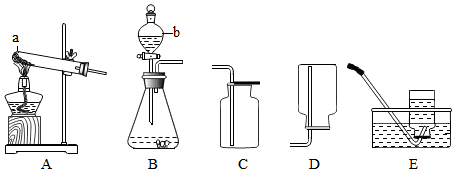
| 实验序号 | ① | ② | ③ | ④ |
| ag大理石 | 块状 | 块状 | 粉末状 | 粉末状 |
| bg盐酸 | 稀盐酸 | 浓盐酸 | 稀盐酸 | 浓盐酸 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
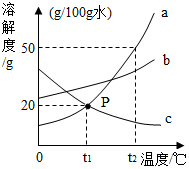 如图是a、b、c三种物质的溶解度曲线,下列分析不正确的是( )
如图是a、b、c三种物质的溶解度曲线,下列分析不正确的是( )| A. | t2℃时a、b、c三种物质的溶解度由大到小的顺序是 a>b>c | |
| B. | t2℃时,将50g a物质放入100g水中充分溶解得到a的饱和溶液(a物质不含结晶水) | |
| C. | 将t2℃时a、b、c三种物质的饱和溶液降温至t1℃时,所得溶液的溶质质量分数关系是b>a=c | |
| D. | t1℃时a的饱和溶液的溶质质量分数为16.7% |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
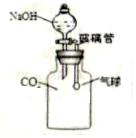 在学习氢氧化钠的性质时,老师将二氧化碳通入盛有氢氧化钠溶液的试管中,同学们没有观察到明显的现象.二氧化碳与氢氧化钠发生了反应吗?探究活动从这个疑问开始.
在学习氢氧化钠的性质时,老师将二氧化碳通入盛有氢氧化钠溶液的试管中,同学们没有观察到明显的现象.二氧化碳与氢氧化钠发生了反应吗?探究活动从这个疑问开始.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 物质 | 丙醇 | 氧气 | 水 | 二氧化碳 | X |
| 反应前质量/g | 6.0 | 12.8 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 7.2 | 8.8 | a |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 过滤时,漏斗里的液体液面要低于滤纸的边缘 | |
| B. | 溶解和过滤操作中,玻璃棒的作用相同 | |
| C. | 蒸发时,将蒸发皿内液体蒸干后停止加热 | |
| D. | 溶解时,在量筒中边加粗盐边搅拌 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com