
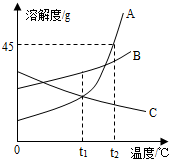
 如图是A、B、C三种物质的溶解度曲线,根据此图回答下列问题:
如图是A、B、C三种物质的溶解度曲线,根据此图回答下列问题:分析 根据题目信息和溶解度曲线可知:A、B两种固体物质的溶解度,都是随温度升高而增大,而C的溶解度随温度的升高而减少;t1℃时,物质A和C的溶解度相等;t2℃时,A物质的溶解度是45g;等质量的A、B、C三种物质的饱和溶液同时从t2℃降温到t1℃,其中溶质质量分数没有发生改变的是C,因为C的溶解度随温度的升高而减少,只是由饱和变为不饱和,质量分数不变;A物质“全部溶解”的原因是因为A物质溶解时,放热引起;析出晶体的原因是:温度降低,A物质的溶解度变小.
解答 解:(1)由溶解度曲线可知:t1℃时,物质A和C的溶解度相等,故答案为:t1;
(2)由溶解度曲线可知:t2℃时,A物质的溶解度是45g;故答案为:45
(3)等质量的A、B、C三种物质的饱和溶液同时从t2℃降温到t1℃,其中溶质质量分数没有发生改变的是C,因为C的溶解度随温度的升高而减少,只是由饱和变为不饱和,质量分数不变;故答案为:C
(4)A物质“全部溶解”的原因是因为A物质溶解时,放热引起;析出晶体的原因是:温度降低,A物质的溶解度变小;故答案为:放热;温度降低,A物质的溶解度变小;
点评 本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液和溶质质量分数的计算,有关的计算要准确,本考点主要出现在选择题和填空题中.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:解答题
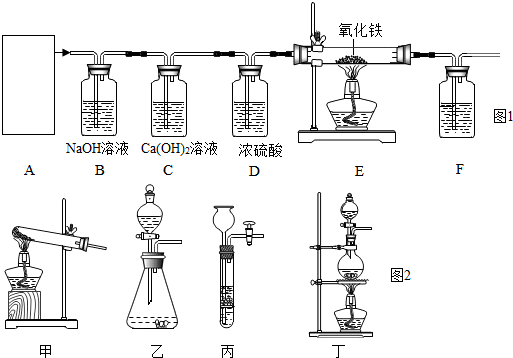
| 玻璃管质量 | 玻璃管及其中固体的质量 | 装置F及其中物质的总质量 | |
| 反应前 | 28.20g | 33.00g | 300.0g |
| 反应后 | 32.84g | 300.4g |
查看答案和解析>>
科目:初中化学 来源:【全国市级联考】山东省寿光市2017届九年级学业水平模拟考试(一模)化学试卷 题型:探究题
化学兴趣小组的同学在探究碱的化学性质时,完成了如下左图所示的两个实验。实验后,小明同学将废液倒入同一废液缸中,发现混合废液浑浊并显红色。请你完成下列问题:
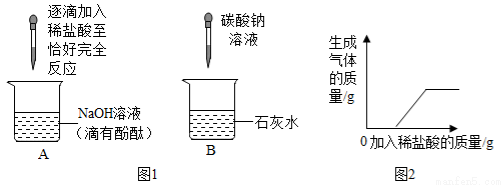
(1)A实验中发生反应的现象为 。
(2)B实验中发生反应的化学方程式是 。
(3)【提出问题】废液中,能使酚酞溶液变红的物质可能是那些呢?
【作出猜想】猜想一:废液中,能使酚酞溶液变红的物质可能是氢氧化钠;
猜想二:废液中,能使酚酞溶液变红的物质还可能是 ;
猜想三:废液中,能使酚酞溶液变红的物质还可能是氢氧化钙;
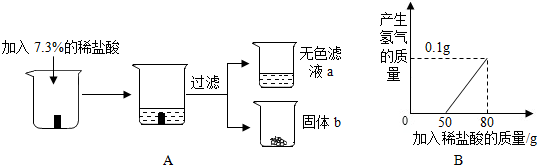
【实验验证】同学们对可能含有的碱性物质进行确定,取一定量的废液过滤,向滤液中逐滴加入稀盐酸,根据反应现象得到了如上右图所示的图像。
【结论】分析图像数据得出,废液中使酚酞溶液变红的物质一定是 ,一定不是 。
【拓展提高】为了使以上废液实现安全排放,你的做法是 。
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验装置 | 实验步骤 | 分析 |
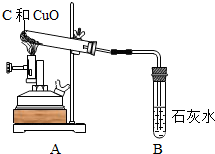 | ①检验装置气密性 | |
| ②把木炭和氧化铜的混合物放入试管,如左图所示连接实验装置 | 装置中存在的问题是B试管处不应该有橡皮塞 | |
| ③改进装置后,点燃酒精喷灯开始实验 | 装置B的作用是检验产物是否有二氧化碳 | |
| ④反应结束时,先将导管从装置B中撤出,再停止加热 | 目的是防止液体倒流引起试管炸裂 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①② | B. | ①④ | C. | ③ | D. | ③④ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com