
| A. | 等质量的CO和CO2,CO和CO2中氧元素的质量比为11:14 | |
| B. | 将溶质质量分数为98%的浓硫酸稀释为49%的硫酸,加水的体积与所取浓硫酸的体积一定相等 | |
| C. | 等质量的NaHCO3和MgCO3分别与足量稀盐酸充分反应,生成CO2的质量相等 | |
| D. | 等质量的质量分数均为4%氢氧化钠溶液与稀硫酸充分反应后,所得溶液显碱性 |
分析 A、根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答;
B、根据将质量分数为98%的浓硫酸稀释为49%的硫酸所加水的质量值分析解答;
C、根据碳元素的质量守恒来完成解答,结合这四种物质与盐酸反应的化学方程式可以知道二氧化碳中的碳元素和碳酸盐中的碳元素的质量相等;设碳酸盐的质量为m,相对分子质量为M,则可以判断碳酸盐中碳元素的质量为:m×$\frac{12}{M}$,根据该计算式可以知道,当碳酸盐的相对分子质量越大,则生成的二氧化碳的质量就越小;
D、根据等质量、等质量分数的硫酸和氢氧化钠两种溶液充分混合后,硫酸与氢氧化钠溶液中所含溶质的质量相等和化学方程式进行解答
解答 解:A、氧元素的质量比为CO:CO2=$\frac{16}{28}:\frac{16×2}{44}$=11:14,故说法正确;
B、溶质的质量可用溶液的质量与溶质的质量分数相乘解得,所以相同温度下,同一物质的饱和溶液与不饱和溶液所含溶质的质量有可能相等(溶液的质量不确定),故B说法错误;
C、分析所给碳酸盐可以知道:M(NaHCO3)=84,M(MgCO3)=84,所以可以判断生成二氧化碳气体的质量相等,故C说法正确;
D、反应中消耗稀硫酸与氢氧化钠的质量比关系如下:
H2SO4+2NaOH═Na2SO4+2H2O
98 80
可知,98份质量的硫酸与80份质量的氢氧化钠恰好完全反应,则等质量、等质量分数的硫酸和氢氧化钠两种溶液充分混合后,氢氧化钠有剩余,溶液显碱性,故D正确;
故选:B.
点评 本题主要考查考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.


科目:初中化学 来源: 题型:选择题
| A. | 金属元素只能显正价 | |
| B. | 在氧气中,氧元素显-2价 | |
| C. | 一种元素在同一种化合物中,可能有几种不同的化合价 | |
| D. | 非金属元素在化合物中总是显负价 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 钴的金属活动性比铜强 | B. | ①为置换反应,②中和反应 | ||
| C. | 氢氧化钴的化学性质稳定 | D. | 氢氧化钴可用来干燥氯化氢气体 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
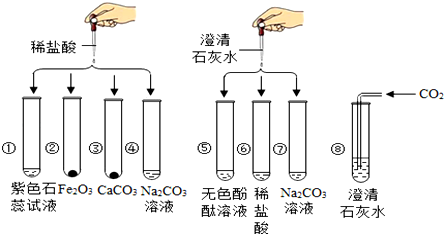
 实验室利用如图所示实验装置进行有关的化学实验,回答下列问题.
实验室利用如图所示实验装置进行有关的化学实验,回答下列问题.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com